
��10�֣���֪��Ӧ��CO
(g) + H2O��g�� CO2 (g) + H2(g)
CO2 (g) + H2(g)
��1����1mol CO��1mol H2O��g������ij�̶��ݻ��ķ�Ӧ������ij�¶��´ﵽƽ�⣺��ʱ��2/3��COת��ΪCO2����÷�Ӧƽ�ⳣ���ı���ʽΪ___ ___,���¶���ƽ�ⳣ��Ϊ ��
��2��������ͬ�����£���������г���1 mol CO2��1 mol H2����ﵽƽ��ʱ�루1����Ƚϣ�
ƽ��Ӧ �ƶ����������Ӧ���������淴Ӧ������������ʱƽ��������CO2���������Լ�����и�ֵ�е� �����ţ�
A. 22.2% B.27.55% C.33.3% D.36.8%
��3��������ͬ�����£���������г���1 mol CO2��1 mol H2��1mol H2O��g������ﵽƽ��ʱ�루1����Ƚϣ�������˵������ȷ���� ������ţ�
��������IJ���һ������ �ڷ�Ӧ���Ũ��һ������
�۷�Ӧ���ת����һ������ ��CO��ƽ�������еİٷֺ���һ������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣���֪��Ӧ��CO(g) + H2O(g)H2(g) + CO2(g) ��H= Q kJ��mol-1����ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 850 |
| ƽ�ⳣ�� | 9.94 | 9 | 1 |
��ش��������⣺
��1���������淴Ӧ��Q 0������ڡ���С�ڡ�����
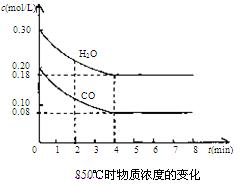
��2��850��ʱ�����Ϊ10L��Ӧ���У�ͨ��һ������CO��H2O��g������������Ӧ��CO��H2O(g)Ũ�ȱ仯����ͼ���Իش�
��0��4 min��ƽ����Ӧ����v(CO)=______ mol/(L��min)
�����б�������Ϊ�ÿ��淴Ӧ�ﵽƽ���־����__________(�����)��
A�������������ܶȱ��ֲ���ʱ
B������Ӧ����0.1molCO(g)ͬʱҲ����0.1molH2O(g)ʱ
C����CO(g)�������������ֲ���ʱ
D�����÷�Ӧ�Ħ�H����ʱ
��3����Ҫ�ӿ�÷�Ӧ���ʣ�ͬʱ��Ҫ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩΪ_____(�����)��
A������ˮ�������� B�������¶�
C��ʹ�ô��� D������ѹǿ E����������CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�캣��ʡ�����и����߿����в��Եػ�ѧ�Ծ� ���ͣ������
��8�֣���֪��Ӧ��CO(g) + H2O(g) H2(g) + CO2(g) ��H=" Q" kJ��mol-1����ƽ�ⳣ�����¶ȵı仯���±���
H2(g) + CO2(g) ��H=" Q" kJ��mol-1����ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 850 |
| ƽ�ⳣ�� | 9.9 4 4 | 9 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ����ר���̵�6�� ��ѧ��Ӧ���ʺͻ�ѧƽ����ϰ���������棩 ���ͣ�ѡ����
��֪��Ӧ����CO(g)��CuO(s)??CO2(g)��Cu(s)�ͷ�Ӧ����H2(g)��CuO(s)  Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ����CO(g)��H2O(g)
Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ����CO(g)��H2O(g)  CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(����)
CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(����)
A����Ӧ����ƽ�ⳣ��K1��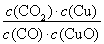
B����Ӧ����ƽ�ⳣ��K��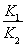
C�����ڷ�Ӧ��������ʱ���¶����ߣ�H2Ũ�ȼ�С����÷�Ӧ���ʱ�Ϊ��ֵ
D�����ڷ�Ӧ�������º����£�����ѹǿ��H2Ũ��һ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�������
��֪��Ӧ��CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
��427��Cʱ��ƽ�ⳣ����9��4�������Ӧ��ʼʱ��һ����̼��ˮ������Ũ�ȶ���0��01mol��L-1������һ����̼�ڴ˷�Ӧ�����µ�ת���ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꺣��ʡ�����и����߿����в��Եػ�ѧ�Ծ� ���ͣ������
��8�֣���֪��Ӧ��CO(g) + H2O(g) H2(g) + CO2(g) ��H= Q kJ��mol-1����ƽ�ⳣ�����¶ȵı仯���±���
|
�¶�/�� |
400 |
500 |
850 |
|
ƽ�ⳣ�� |
9.94 |
9 |
1 |
��ش��������⣺
��1���������淴Ӧ��Q 0������ڡ���С�ڡ�����
��2��850��ʱ�����Ϊ10L��Ӧ���У�ͨ��һ������CO��H2O��g������������Ӧ��CO��H2O(g)Ũ�ȱ仯����ͼ���Իش�
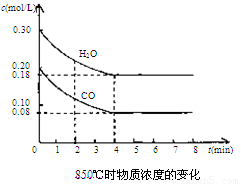
��0��4 min��ƽ����Ӧ����v(CO)=______ mol/(L��min)
�����б�������Ϊ�ÿ��淴Ӧ�ﵽƽ���־����__________(�����)��
A�������������ܶȱ��ֲ���ʱ
B������Ӧ����0.1molCO(g) ͬʱҲ����0.1molH2O(g)ʱ
C����CO(g)�������������ֲ���ʱ
D�����÷�Ӧ�Ħ�H����ʱ
��3����Ҫ�ӿ�÷�Ӧ���ʣ�ͬʱ��Ҫ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩΪ_____(�����)��
A������ˮ�������� B�������¶�
C��ʹ�ô��� D������ѹǿ E����������CO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com