
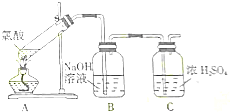
���� ��1�����������ȷֽ�����O2��Cl2��Cl2Ϊ����ɫ���壬����A��������ɫ�ж����ɺ���������
�������ܺ�ˮ��Ӧ����HCl��HClO�����������ܺͼ���Һ��Ӧ��Ũ���������ˮ�ԣ��ܸ������壻
������������ȼ�ԣ������ô����ǵ�ľ�����飻
��2��Ũ�Ƚϸߵ�������ͭ��Ӧ������ClO2���壬Cu����������Cu 2+���÷�Ӧ��ClԪ�ػ��ϼ���+5�۱�Ϊ+4�ۡ�CuԪ�ػ��ϼ���0�۱�Ϊ+2�ۣ�����ת�Ƶ����غ���ƽ����ʽ��
��� �⣺��1�����������ȷֽ�����O2��Cl2��Cl2Ϊ����ɫ���壬���A������ʻ���ɫ�����Կ�����������A������ʻ���ɫ���ɴ˿�֪����ֽ�IJ����к���Cl2��
�ʴ�Ϊ����������ɫ���壻Cl2��
�������ܺ�ˮ��Ӧ����HCl��HClO�����������ܺͼ���Һ��Ӧ����B������������������Ũ���������ˮ�ԣ��ܸ������壬����C�������Ǹ������壬
�ʴ�Ϊ�������������������壻
������������ȼ�ԣ������ô����ǵ�ľ�����飬���Լ�����һ������ķ����ǣ��������ǵ�ľ��������C�ij����ڣ���������ǵ�ľ����ȼ��֤�����������ɣ�
�ʴ�Ϊ���������ǵ�ľ��������C�ij����ڣ�
��2��Ũ�Ƚϸߵ�������ͭ��Ӧ������ClO2���壬Cu����������Cu 2+���÷�Ӧ��ClԪ�ػ��ϼ���+5�۱�Ϊ+4�ۡ�CuԪ�ػ��ϼ���0�۱�Ϊ+2�ۣ�ת�Ƶ�����Ϊ2������ת�Ƶ����غ���ƽ����ʽΪCu��2ClO3-+4H+=Cu2++2ClO2��+2H2O��
�ʴ�Ϊ��2ClO3-+4H+=Cu2++2ClO2��+2H2O��
���� ���⿼�����ʳɷֲⶨ��Ϊ��Ƶ���㣬�漰ʵ�������жϡ�������顢���ӷ���ʽ����д��֪ʶ�㣬��ȷ���������ǽⱾ��ؼ���֪������װ�����ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3���������������� | B�� | ƽ��������Ӧ�����ƶ� | ||
| C�� | ƽ�����淴Ӧ�����ƶ� | D�� | ���淴Ӧ���ʶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2����������NaOH�ǻ�ԭ�� | |
| B�� | ��������Clԭ�Ӻͱ���ԭ��Clԭ�ӵ����ʵ����ı�Ϊ5��1 | |
| C�� | ÿ����1mol��NaClO3ת��6mol�ĵ��� | |
| D�� | Cl2�������������ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
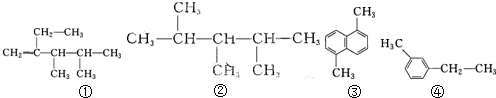
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5L1.2mol•L-1��Na2SO4��Һ | B�� | 2L 0.8mol•L-1��Na0H��Һ | ||
| C�� | 1L1mol•L-1��Na2CO3��Һ | D�� | 4L 0.5mol•L-1��NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
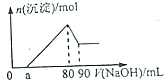 Fe2O3��Al2O3�Ļ������ȫ�ܽ���160mL2mol/LHCl��Һ�У���������Һ�еμ�NaOH��Һ�õ���ͼ������˵������ȷ���ǣ�������
Fe2O3��Al2O3�Ļ������ȫ�ܽ���160mL2mol/LHCl��Һ�У���������Һ�еμ�NaOH��Һ�õ���ͼ������˵������ȷ���ǣ�������| A�� | ��a=20mLʱ����������Fe2O3ռ0.02mol | |
| B�� | ���μӵ�Na0H��Һ��Ũ��Ϊ4mol/L | |
| C�� | a�㴦��Na0H��Һ�����Ϊa��50mL | |
| D�� | ��a=20mL����ʣ����������Ϊ20mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 15 �� | B�� | 16 �� | C�� | 17 �� | D�� | 18 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com