
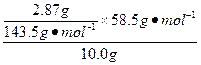 ×100%=11.7%
×100%=11.7%

科目:高中化学 来源:不详 题型:单选题
| A.都是碱性氧化物 | B.都具有强氧化性 |
| C.都能和H2O、H+反应 | D.和二氧化碳反应生成同种物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②① | B.②①③ | C.②③⑤ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2S和S | B.Na2O和Na2S | C.Na2O2和Na2S | D.Na2O2和Na2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.消耗盐酸一样多 | B.放出CO2一样多 |
| C.消耗盐酸前者多 | D.放出的CO2,第一份为第二份的一半 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com