
请回答下列问题:?
(1)铁屑表面少量的铁锈(主要成分为Fe2O3·aH2O)对制取硫酸亚铁有无影响 (填“有”或“无”)。其原因是: 。如有影响将如何操作? (若无影响,此问可以不答)。
(2)FeSO4在不同温度下的溶解度如下表所示:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |
由于废铁屑含有C、Si等杂质,为了使FeSO4溶液的浓度增大,便于反应后分离溶液和残渣,该小组实验时采取了水浴加热和趁热过滤的方法。这样做的主要目的是为了防止 。你认为实验时的水浴温度最好控制在 ℃?左右。??
(3)测定晶体中结晶水含量所用的实验仪器除托盘天平(或物理天平)、研钵、坩埚、坩埚钳、三脚架、泥三角、酒精灯、药匙外,还有 ;判断晶体中结晶水完全失去的实验操作是 。?
(4)计算硫酸亚铁晶体化学式中x的实验值表达式为x= ?。(已知:硫酸亚铁晶体中结晶水的质量为m g、硫酸亚铁晶体的质量为w g)?
(5)由于铁屑或铁丝与硫酸反应速率慢,实验过程中有的同学提出采用电解的方法,可以加快制取FeSO4溶液的反应速率,该方法的电解质溶液是 ,阳极的电极反应方程式为: 。?
请你再写出一种(不包括改变温度和硫酸的浓度)以铁单质为反应物,能加快制取FeSO4溶液反应速率的方法: 。?
(1)无Fe2O3·xH2O与H2SO4反应生成Fe3+,过量的铁屑可以将Fe3+?还原成Fe2+,只要保证铁屑过量,就可以排除铁锈的影响 ???
(2)析出硫酸亚铁晶体与残渣一起被过滤掉(或硫酸亚铁晶体析出)60
(3)玻璃棒、干燥器连续两次加热、冷却、称量的质量差不超过0.1 g
(4)x =![]() ?
?
(5)稀硫酸 阳极:Fe - 2e- = Fe2+??
增大反应物接触面积:用铁粉与稀硫酸反应;利用原电池原理:用铁与铜(或CuSO4溶液,C粉等)和稀硫酸反应?
增加阳离子的氧化性:用过量的铁粉与CuSO4溶液或Fe2(SO4)3溶液等反应(3分,其他合理答案参照给分)?
解析:(1)无影响,因铁锈Fe2O3·aH2O + 6H += 2Fe3++(a+3)H2O,2Fe3++ Fe=3Fe2+?,只要Fe量大即无影响。?
(2)FeSO4的溶解度在60 ℃较大,故可在60 ℃过滤,防止低温下析出的FeSO4和C、Si等杂质一并过滤掉。?
(3)将FeSO4·xH2O 在坩埚中加热后应在干燥器中冷却以防止再结合水,故缺玻璃棒(搅拌用)和干燥器。是否完全失水的判断方法是连续两次加热、冷却、称量,其质量差不超过0.1 g。?
(4)FeSO4·xH2O= FeSO4 + xH2O?
152+18x 18x?
w m?
x =![]() ??
??
(5)要使Fe转化为Fe2+?,故Fe必作阳极,电解溶液为H2SO4。?
(6)可利用Fe作原电池负极的方法加快反应。?
如加入CuSO4溶液、或加入单质铜、或加入碳粉等。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:


| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外活动小组在实验室设计了如下图所示的实验装置,进行“氨的催化氧化”实验。
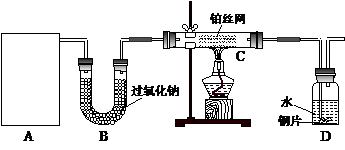
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①硝酸铵;②碳酸铵;③碳酸氢铵;④氯化铵;⑤熟石灰;⑥氢氧化钠。
若A中制取气体时只用了一种药品,则该药品可以是_______________(填选项编号),在只用一种药品制取氨气时,图中空白处所需仪器应为____________________(选填下列仪器编号,固定装置省略)。
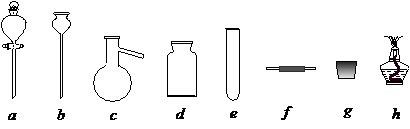
(2)该装置补充完整后,仍然存在一定缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①______________________________________________________________________;
②______________________________________________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用__________________________________________________________;
②写出C中发生反应的化学方程式:_________________________________________;
③若A、B处试剂足量,则装置D中可以观察到的实验现象有_____________________。
查看答案和解析>>
科目:高中化学 来源:上海市闵行区2010届高三第二次模拟考试化学试卷 题型:实验题
(12分)某化学课外活动小组在实验室设计了如下图所示的实验装置,进行“氨的催化氧化”实验。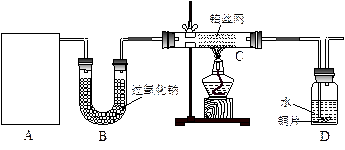
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①硝酸铵;②碳酸铵;③碳酸氢铵;④氯化铵;⑤熟石灰;⑥氢氧化钠。
若A中制取气体时只用了一种药品,则该药品可以是_______________(填选项编号),在只用一种药品制取氨气时,图中空白处所需仪器应为____________________(选填下列仪器编号,固定装置省略)。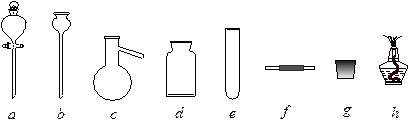
(2)该装置补充完整后,仍然存在一定缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①______________________________________________________________________;
②______________________________________________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用__________________________________________________________;
②写出C中发生反应的化学方程式:_________________________________________;
③若A、B处试剂足量,则装置D中可以观察到的实验现象有_____________________。
查看答案和解析>>
科目:高中化学 来源:上海市闵行区2010届高三第二次模拟考试化学试卷 题型:实验题
(12分)某化学课外活动小组在实验室设计了如下图所示的实验装置,进行“氨的催化氧化”实验。
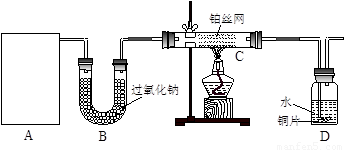
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①硝酸铵;②碳酸铵;③碳酸氢铵;④氯化铵;⑤熟石灰;⑥氢氧化钠。
若A中制取气体时只用了一种药品,则该药品可以是_______________(填选项编号),在只用一种药品制取氨气时,图中空白处所需仪器应为____________________(选填下列仪器编号,固定装置省略)。
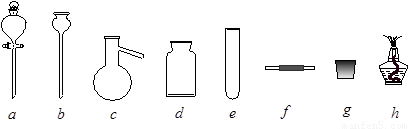
(2)该装置补充完整后,仍然存在一定缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①______________________________________________________________________;
②______________________________________________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用__________________________________________________________;
②写出C中发生反应的化学方程式:_________________________________________;
③若A、B处试剂足量,则装置D中可以观察到的实验现象有_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com