
分析 食物的酸碱性与化学上所指的溶液的酸碱性是不同的概念,它是指食物成酸性或成碱性,是按食物在体内代谢最终产物的性质来分类的;蛋白质是常见的酸性食物;正常人血浆的PH值为7.35~7.45;蛋白质在体内经过消化、吸收后,最后氧化成酸,是常见的酸性食物;蔬菜、水果含钾、钠、钙、镁等盐类,在人体内代谢后生成碱性物质,使体液呈弱碱性.
解答 解:酸性食物和碱性食物是根据食物在人体内消化后终端产物的酸碱性来划分的,而不是食物本身的酸碱性,通常,富含S、Cl、P、N等非金属元素的食物进入体内,通过转化后会产生酸性物质,而富含K、Ca、Na、Fe、Zn、Mg等金属元素的食物进入体内,通过转化后产生碱性物质.
鸡蛋、猪瘦肉在体内经过消化、吸收后,最后氧化成酸,是常见的酸性食物;
血液分为血浆和血细胞两部分,正常人血浆的PH值为7.35~7.45,所以人的血液呈弱碱性;
我国居民形成了摄入蔬菜和水果偏少的习惯,蛋白质摄入偏多,蛋白质在体内经过消化、吸收最后氧化成酸,一般尿液呈酸性,
故答案为:鸡蛋;猪瘦肉;弱碱性;酸.
点评 本题考查了食物的酸碱性判断,注意食物的酸碱性是根据食物在体内代谢最终产物的性质来分类,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子序数 d>c>b>a | B. | 原子半径 A>B>D>C | ||
| C. | 离子半径 C2->D->B+>A2+ | D. | 阴离子的还原性C2-<D- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol•L-1CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 将CH3COONa溶液从20℃升温至30℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| C. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(C{l}^{-})}$>1 | |
| D. | 0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓的强酸和稀的强碱反应 | B. | 浓的弱酸和稀的强碱反应 | ||
| C. | 等浓度的强酸和弱碱反应 | D. | 稀的强酸和浓的弱碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
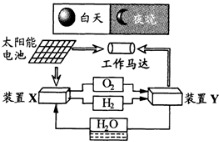
| A. | 装置X能实现燃料电池的燃料和氧化剂再生 | |
| B. | 装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 装置X是原电池,装置Y是电解池 | |
| D. | 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当b<a时,发生的离子反应为:CO2+2OH-=H2O+CO32- | |
| B. | 当b=l.5a时,发生的离子反应为:Ba2++2CO2+3OH-=H2O+BaCO3↓+HCO3- | |
| C. | 当b=2a时,发生的离子反应为:2Ba2++3CO2+6OH-=3H2O+2BaCO3↓+CO32- | |
| D. | 当b>3a时,发生的离子反应为:CO2+OH-=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl=Na++Cl- | B. | H2SO4=2H++SO42- | ||
| C. | Ca(OH)2=Ca2++2OH- | D. | Al2(SO4)3=Al3++SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com