
A、氮分子的电子式: |
B、硫原子的结构示意图: |
C、NH4Cl的电子式: |
D、水分子的结构式: |
 故A错误;
故A错误; ,故B错误;
,故B错误;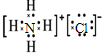 ,故C错误;
,故C错误;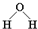 ,故D正确;
,故D正确;

 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 原子半径(nm) | 0.066 | 0.104 | 0.117 | 0.137 |
| 常况下单质色态 | 无色气体 | 淡黄色固体 | 灰色固体 略带金属光泽的 | |
| 主要单质熔点(℃) | -218.4 | 113 | 217 | 450 |
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知I、II反应在一定条件节焓变及平衡常数如下:
已知I、II反应在一定条件节焓变及平衡常数如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①②③ |
| C、①②⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v正(N2)=v 逆(NH3) |
| B、3v正(N2)=v 正(H2) |
| C、2v正(H2)=3v 逆(NH3) |
| D、v正(N2)=3v 逆(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某小组同学利用右图所示装置探究氨气的性质.
某小组同学利用右图所示装置探究氨气的性质.查看答案和解析>>
科目:高中化学 来源: 题型:
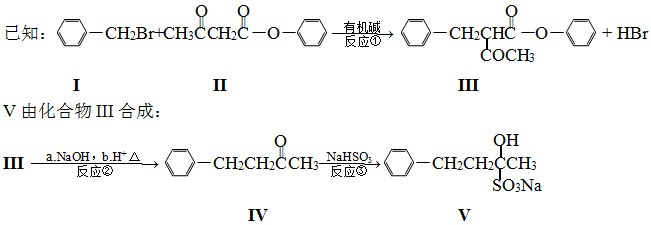
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=6的某溶液 |
| B、加酚酞后显无色的溶液 |
| C、能与金属Al反应放出H2的溶液 |
| D、c(H+)>c(OH-)的任意水溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com