
反应C (S) +H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对反应速率几乎无影响的是( )
A.增加C的量 B.将容器的体积缩小一半
C.保持体积不变,充入N2 使体系压强增大
D.保持压强不变,充入N2 使容器体积变大
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
②2H2(g)+O2(g) ![]() 2H2O(g) ΔH=-483.6 kJ·mol-1??
2H2O(g) ΔH=-483.6 kJ·mol-1??
则制备水煤气的反应C(s)+H2O(g) ![]() CO(g)+H2(g) ΔH为( )?
CO(g)+H2(g) ΔH为( )?
A.262.6 kJ·mol-1?? B.-131.3 kJ·mol-1??
C.-352.3 kJ·mol-1?? D.131.3 kJ·mol-1??
查看答案和解析>>
科目:高中化学 来源:2012届山东省济南市高三12月月考化学试卷 题型:填空题
(15分)能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则CH4燃烧的热化学方程式为__________________________________________。
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-437.3 kJ·mol-1
H2(g)+O2(g)===H2O(g);ΔH=-285.8 kJ·mol-1
CO(g)+O2(g)===CO2(g);ΔH=-283.0 kJ·mol-1
则煤气化反应C(s)+H2O(g)===CO(g)+H2(g)的焓变ΔH=________kJ·mol-1。
(3)如下图所示组成闭合回路,其中,甲装置中CH4为负极,O2和CO2的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200 mL。
①甲装置中气体A为 (填“CH4”或“O2和CO2”),d极上的电极反应式为_____________。
②乙装置中a极上的电极反应式为____________________________。
若在a极产生112mL(标准状况)气体,则甲装置中消耗CH4________ mL (标准状况),乙装置中所得溶液的pH=__________。(忽略电解前后溶液体积变化)
③如果乙中电极不变,将溶液换成饱和Na2SO4溶液,当阴极上有a mol气体生成时,同时有w g Na2SO4·10H2O晶体析出,若温度不变,剩余溶液中溶质的质量分数应为________(用含w、a的表达式表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源:2011届江苏省宿豫中学高三第二次模拟考试化学试卷 题型:填空题
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。
⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH= ▲ 。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH= ▲ 。(用含ΔH1、ΔH2的代数式表示)
⑵CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。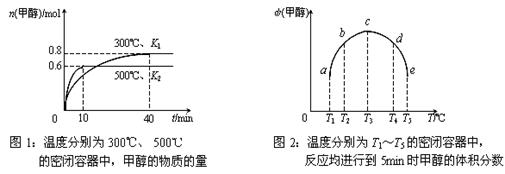
①该反应的ΔH3 ▲ 0(选填“<”、“>”或“=”,下同),K1 ▲ K2。
②将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有 ▲ 。
⑶某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式: ▲ 。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省高三高考压轴化学试卷 (带解析) 题型:填空题
(14分)碳酸锶广泛应用于电子工业。以天青石(主要成分为SrSO4)为基本原料制备碳酸锶。
(1)碳还原法制备。
①已知:SrSO4(s) + 4C(s)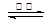 4CO(g) + SrS(s) △H=+a kJ·mol-1
4CO(g) + SrS(s) △H=+a kJ·mol-1
SrSO4(s) + 2C(s)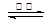 2CO2(g) + SrS(s) △H=+b kJ·mol-1
2CO2(g) + SrS(s) △H=+b kJ·mol-1
则:反应C(s) + CO2(g)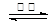 2CO(g)的△H= ___________kJ·mol-1。
2CO(g)的△H= ___________kJ·mol-1。
②SrS是强碱弱酸盐,热水中发生水解的化学反应方程式为_______________________。
③水解所得Sr(OH) 2与NH4HCO3按照物质的量比1:1投料制备SrCO3,则化学反应方程式为__________________________________________________。
(2)湿法制备。(已知:Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.1×10-10。)
①将天青石矿粉与Na2CO3溶液搅拌混匀、加热,发生的离子反应方程式为: ____________。
②当转化完成时,混合液中c(CO32-)= 1.0×10-3mol/L,c(SO42-)=______________mol/L。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省忻州市高三第一次联考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.铅蓄电池在放电过程中,正负极质量均增加
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H> O
C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.将浓度为0.1mol·L-1的HF溶液加水不断稀释,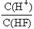 的值始终保持增大
的值始终保持增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com