
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。
从废料中回收氧化钴(CoO)的工艺流程如下: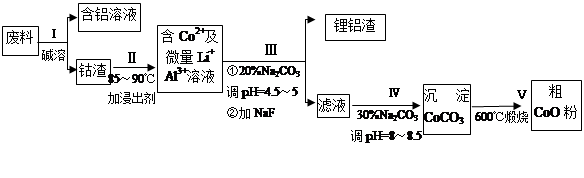
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 。
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为(产物中只有一种酸根) 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因_______________。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式____________________。
(4)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是__________。
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是______(填序号)。
| A.c(Na+) = 2c(CO32-) |
| B.c(Na+) > c(CO32-) > c(HCO3-) |
| C.c(OH-) > c(HCO3-) > c(H+) |
| D.c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3) |
(共14分)
(1)2Al+2OH-+2H2O = 2AlO- 2+3H2↑
(2)4Co2O3·CoO + Na2S2O3 + 11H2SO4 = 12CoSO4 + Na2SO4 + 11H2O
Co2O3·CoO可氧化盐酸产生Cl2,污染环境。(合理即可)
(3)2Al3++3CO2- 3+3H2O = 2Al(OH)3↓+3CO2↑
(4)调整pH,提供CO2- 3,使Co2+沉淀为CoCO3
(5)B C D (有错不得分,答对2个得1分,全对得2分)
(6)CoCl2?2H2O
解析试题分析:
(1)铝和氢氧化钠溶液反应:2Al+2OH-+2H2O = 2AlO2-+3H2↑
(2)①酸根应为硫酸根,根据溶液中离子可得方程式:4Co2O3·CoO + Na2S2O3 + 11H2SO4 = 12CoSO4 + Na2SO4 + 11H2O;盐酸中氯具有一定还原性,Co2O3·CoO可氧化盐酸产生Cl2,污染环境。
(3)发生双水解:2Al3++3 CO2- 3+3H2O = 2Al(OH)3↓+3CO2↑。
(4)调整pH,提供CO2- 3,使Co2+沉淀为CoCO3
(5)CO2- 3会部分水解:CO2- 3+H2O HCO3-+OH–,HCO3-+H2O
HCO3-+OH–,HCO3-+H2O H2CO3+OH- A、 c(Na+) >2c(CO2- 3),错误;B 、c(Na+) > c(CO2- 3) > c(HCO3-),正确;C 、c(OH-) > c(HCO3-) > c(H+),正确;D、质子守恒: c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3),正确。
H2CO3+OH- A、 c(Na+) >2c(CO2- 3),错误;B 、c(Na+) > c(CO2- 3) > c(HCO3-),正确;C 、c(OH-) > c(HCO3-) > c(H+),正确;D、质子守恒: c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3),正确。
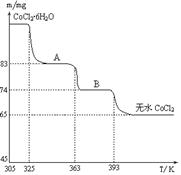
(6)最终无水的m(CoCl2)=65mg,M(CoCl2)=130g/mol,所以n(CoCl2)=0.5×10-3mol,从A到无水氯化钴减少m(H2O)="18mg," n(H2O)=1×10-3mol,可知N(CoCl2):N(H2O)=1:2,为CoCl2?2H2O。
考点:本题以工业流程为载体考查元素及其化合物性质、方程式书写、电解质溶液、化学计算等相关知识。。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:填空题
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂
质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。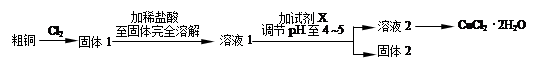
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
① 仪器A的名称是 。
② 装置B中发生反应的离子方程式是 。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要
(填“是”或“否”) 。
(2)试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号) 。
a.NaOH b.NH3·H2O c.CuO d.Cu2(OH) 2CO3 e.CuSO4
(3)在溶液2转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) +4Cl-(aq) CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)
蓝色 绿色
① 上述反应的化学平衡常数表达式是K= 。若增大氯离子浓度,K值(填“增大”、“减小”或“不变”) 。
② 取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号) 。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、V、W是元素周期表前四周期中的五种常见元素,其相关信息如下表;
| 元素 | 相关信息 |
| X | X是形成化合物种类最多的元素,它的一种气态氧化物能产生温室效应 |
| Y | Y是地壳中含量最多的元素 |
| Z | Z和Y形成的一种化合物Z2Y2为淡黄色粉末,可作为呼吸面具里氧气的来源 |
| V | V的单质是淡黄色固体,是黑火药的一种主要成分 |
| W | W的单质是人们最早发现和使用的金属之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 、
、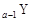 、
、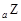 、
、 、
、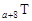 是五种常见的短周期元素,其原子半径随原子序数变化如下图所示。Z是地壳中含量最高的元素。W原子最外层电子数是K层电子数的2倍。
是五种常见的短周期元素,其原子半径随原子序数变化如下图所示。Z是地壳中含量最高的元素。W原子最外层电子数是K层电子数的2倍。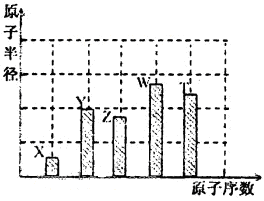
(l)W在周期表中的位置为_______________________。
(2)Y、Z的10电子氢化物分子中均含有的化学键类型为___________;其稳定性较强的是___________
(填化学式)。
(3)用化学方程式表示YZ2形成酸雨的反应:______________________。
用精密pH试纸(精确到0.l)测定酸雨pH的操作是______________________。
(4)常温下用1 mol/L100 mL NaOH溶液恰好完全吸收0.1molTZ2气体,此反应的离子方程式为
______________________;此时溶液pH<7的原因是___________________________。
(5)在25℃、101kPa下,己知W与X形成的气态化合物与足量Z2点燃完全反应(生成W的最高价
化合物),恢复至原状态,平均每转移l mol e_放热190 kJ,该反应的热化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
周期表中短周期6种元素A、B、C、D、E、F,原子序数依次增大。A的原子半径最小,A和D、C和F分别同主族,F的单质是黄色固体,B所形成的化合物种类最多,E的最外层电子数等于其电子层数。
(1)写出工业制备E单质的化学方程式____________________。
(2)写出一种由其中两种元素组成的既含极性键又含非极性键的18电子微粒________(写化学式)。
(3)由A、C元素组成的化合物甲与由D、C元素组成的化合物乙反应可制备O2,请写出乙的电子式__________。
(4)3mol DABC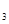 和2mol D
和2mol D C
C 混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分及物质的量分别是____________________。
混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分及物质的量分别是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
用如图所示装置进行实验(夹持装置已略去)。请回答下列问题: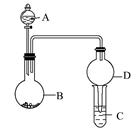
(1)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。将浓硝酸滴入B中,则B中发生反应的化学方程式为。
(2)若A中为浓氨水,B中为生石灰,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,原因可能是(填序号)。
a.生石灰和浓氨水反应产生氨气,氨气易溶于水
b.生石灰和水反应,消耗水,使氨气的溶解量减少
c.反应放出大量热,使氨气在水中的溶解度明显降低
②C中通入过量氨气时,相应的离子方程式为。
(3)若A中为水,B中为过氧化钠,C中为酸性淀粉碘化钾溶液,将水滴入B中后,B中的实验现象为;若C中溶液变为蓝色,则C中发生反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
随着卤素原子半径的增大,下列递变规律正确的是
| A.单质的熔点逐渐降低 | B.卤素离子还原性逐渐增强 |
| C.气态氢化物稳定性逐渐增强 | D.单质氧化性逐渐增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com