
 H++HO2-
H++HO2-

科目:高中化学 来源:不详 题型:填空题






查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 操作 | 现象 | 结论 |
| A | 将Cl2通入KI溶液 | 溶液变蓝色 | I-的还原性强于Cl- |
| B | 常温下将Fe片放入浓硫酸中 | 无明显变化 | 可以用铁槽车装运浓硫酸 |
| C | 将一小块Na放入硫酸铜溶液中 | 有红固体析出 | Na的活泼性强于铜 |
| D | 向AgCl浊液中滴加Na2S溶液 | 黑色沉淀生成 | Ksp(AgCl)>Ksp(Ag2S) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
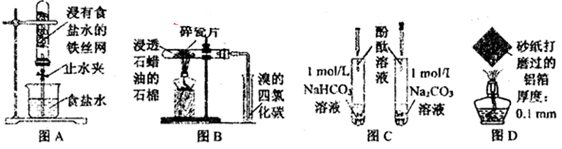
| A.图A,一段时间后打开止水夹,观察到导管中液面上升,因为铁发生了吸氧腐蚀 |
| B.图B,加热一段时间,观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生 |
| C.图C,溶液均变红,碳酸钠溶液颜色较深,因为相同条件下水解能力HCO3-强于CO32- |
| D.图D,加热一段时间,观察到熔化的铝未滴落,因为铝表面生成氧化铝的熔点很高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.用图1所示的装置做喷泉实验时观察到产生白色喷泉 |
| B.如图2所示的两套装置均可制备NH3(不考虑净化和收集) |
| C.称取2.5 g CuSO4·5H2O,放入100 mL容量瓶中,配制0.10 mol·L-1CuSO4溶液 |
| D.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验方案 |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1mol/L NaOH溶液中先加入3滴1 mol/L MgCl2溶液,再加入3滴1 mol/L FeCl3溶液 |
| C | 检验蔗糖的水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入适量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
| D | 测定铝箔中氧化铝的含量 | 取a g铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰后,测其体积为b L(已转化为标准状况下) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 事实 | 结论 |
| A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| B | HCl与Na2CO3溶液反应生成CO2 | 可用饱和Na2CO3溶液除去CO2中的少量HCl |
| C | 氧化铜高温下生成红色物质,该物质可与稀硫酸反应 | 氧化铜高温下可分解生成Cu2O |
| D | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com