

| A. | (1)图显示M中只有一种溶质且为Na2CO3 | |
| B. | (3)图显示M中有两种溶质且为Na2CO3.NaOH | |
| C. | (2)图显示M中有两种溶质且为Na2CO3.NaHCO3 | |
| D. | (4)图显示M中c(NaHCO3)=c(Na2CO3) |
分析 发生反应为:NaOH+HCl=NaCl+H2O,Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+CO2+H2O,由方程式可知碳酸钠转化为碳酸氢钠消耗盐酸与碳酸氢钠反应消耗盐酸体积相等,
图(1)中加入盐酸即有CO2生成,说明溶质只有一种,即NaHCO3;
图(2)中OA<AB,说明溶液M中含有Na2CO3和NaHCO3两种溶质;
图(3)中OA=AB,说明溶质只有Na2CO3;
图(4)中OA>AB,说明溶液M中含有NaOH和Na2CO3两种溶质,以此解答.
解答 解:发生反应为:NaOH+HCl=NaCl+H2O,Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+CO2+H2O,由方程式可知碳酸钠转化为碳酸氢钠消耗盐酸与碳酸氢钠反应消耗盐酸体积相等,
A.图(1)中加入盐酸即有CO2生成,说明溶质只有一种,即NaHCO3,故A错误;
B.图(3)中OA=AB,说明溶质只有Na2CO3,发生Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+CO2+H2O,故B错误;
C.图(2)中OA<AB,说明溶液M中含有Na2CO3和NaHCO3两种溶质,故C正确;
D.图(4)中OA>AB,说明溶液M中含有NaOH和Na2CO3两种溶质,不存在NaHCO3,故D错误.
故选C.
点评 本题主要考查了图象和数据的分析及根据化学方程式进行计算,侧重于学生的分析能力和计算能力的考查,注意守恒法在解答中的应用,需明确反应后溶质的可能成分来比较,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
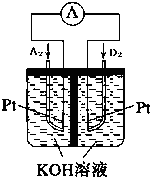 A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①② | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
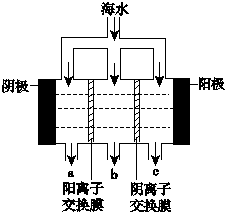 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2NH3=2NaNH2+H2↑ | B. | NH3+HCl=NH4Cl | ||
| C. | 4NH3+6NO=5N2+6H2O. | D. | 3SiH4+4NH3=Si3N4+12H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| D. | CO2(g)+2NaOH(l)═2NaHCO3(l)△H=-(8x-2y) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸一般要保存棕色试剂瓶中,置于阴凉处,原因是:4HNO3$\frac{\underline{\;见光或受热\;}}{\;}$2NO2↑+O2↑+2H2O | |
| B. | 配制240ml浓度为1 mol•L-1的NaOH溶液,需将NaOH固体放在烧杯中,用托盘天平称取10.00g,选用250ml的容量瓶进行配制 | |
| C. | 常温下可用铁质或铝制容器储运浓硝酸,是因为常温下二者不发生反应 | |
| D. | 铵盐在加热时都会分解产生氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com