分析:A、过氧化钠是离子化合物,由钠离子与过氧根离子构成.
B、氯化镁是离子化合物,由镁离子和氯离子构成,只含有离子键,不含共价键.
C、氮元素存在同位素.
D、氯原子的1个电子形成氯离子,质子数不变,根据核外电子排布书写结构示意图.
解答:解:A、过氧化钠是离子化合物,由钠离子与过氧根离子构成,电子式为
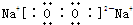
,故A错误;
B、氯化镁是离子化合物,由镁离子和氯离子构成,只含有离子键,不含共价键,故B错误;
C、氮元素存在同位素,氮原子中,质子数为7,中子数不一定为7,故C正确
D、氯原子的1个电子形成氯离子,质子数不变为17,核外电子数为18,结构示意图为

,故D错误.
故选:C.
点评:考查常用化学用语,难度较小,注意注意常用化学用语的书写,离子和原子、分子电子式的不同.

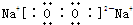 ,故A错误;
,故A错误; ,故D错误.
,故D错误.
