
分析 根据n=$\frac{Wg}{Mg/mol}$×NA先计算出阿伏伽德罗常数NA,32S的一个原子的质量为$\frac{32}{{N}_{A}}$,以此进行计算.
解答 解:Wg某元素(无同位素)所含原子数目为n,该元素原子的摩尔质量为Mg/mol,
则$\frac{Wg}{Mg/mol}$×NA=n,NA=$\frac{nM}{W}$,
32S的一个原子的质量为:$\frac{32}{{N}_{A}}$=$\frac{32W}{nM}$g,
故答案为:$\frac{32W}{nM}$g.
点评 本题考查物质的量的有关计算,题目难度不大,把握质量、物质的量、微粒数目的关系为解答的关键,注重基础知识的考查,培养了学生的化学计算能力.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | A | B | C | D |
| 实验 方案 | 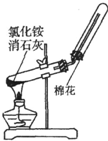 | 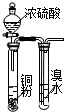 | 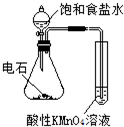 |  置于光亮处 |
| 实验 目的 | 制取并收集氨气 | 验证浓硫酸的强氧化性 | 验证乙炔的还原性 | 验证甲烷与氯气发生 化学反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
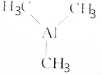 )可用于金属有机化合物气相沉积,下列有关说法正确的是( )
)可用于金属有机化合物气相沉积,下列有关说法正确的是( )| A. | 三甲基铝的摩尔质量是72 | |
| B. | 14.4g三甲基铝中碳原子数为0.6NA | |
| C. | 0.5mol三甲基铝的质量为36g•mol-1 | |
| D. | 1mol三甲基铝在标准状况下的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下$\frac{c({H}^{+})}{c({OH}^{-})}$=1012的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| B. | 含有大量Al3+的溶液中:Na+、NH4+、Cl-、HCO3- | |
| C. | 能使pH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- | |
| D. | 常温下,由水电离出的c(H+)=1×10-13 mol•L-1的溶液中:K+、Fe3+、CH3COO-、SO42-电解 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com