
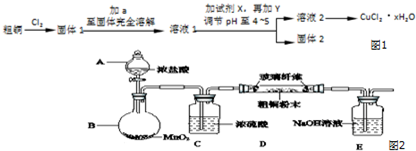
分析 粗铜中含有Fe,与氯气反应生成CuCl2和FeCl3,为防止水解,应加入过量的稀盐酸进行溶解,并保证金属完全反应,溶液1中的金属离子有Fe3+、Fe2+、Cu2+,加入试剂X目的是将溶液中Fe2+氧化为Fe3+,应为H2O2,还原得到水,是绿色氧化剂,通过调节pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且加入Y可以消耗氢离子且不能引入新杂质,可以为CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3.滤液经过加热浓缩、冷却结晶、过滤、洗涤、干燥得到CuCl2•2H2O.
(1)Fe2+具有还原性,可以使酸性高锰酸钾溶液褪色;能与K3[Fe(CN)6]反应得到蓝色铁氰化亚铁蓝色沉淀;
加入试剂X目的是将溶液中Fe2+氧化为Fe3+,最好应为H2O2;
(2)调节pH至4~5之间,液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀,过滤分离;得到固体2的操作是将不溶固体与液体进行分离;
(3)B装置中二氧化锰与浓盐酸在加热条件下反应生成氯气,C装置干燥氯气,D装置中粗铜(Fe、Cu的混合物)与氯气反应生成CuCl2和FeCl3,多于的氯气用氢氧化钠溶液吸收,以防污染空气,由于HCl不影响氯气和粗铜的反应的产物,且可以抑制氯化铜水解,氯气中混有的HCl不需要除去;
(4)①平衡常数为生成物浓度化学计量数次数幂乘积与反应物浓度化学计量数次数幂乘积的比值;
平衡常数只受温度影响,与离子浓度无关;
②稀溶液中以Cu(H2O)42+为主,呈蓝色,浓溶液中以CuCl42-为主,呈黄色,一定浓度下呈蓝绿色,结合平衡移动原理分析;
(5)CuCl2•xH2O晶体加热容易分解,且氯化铜易水解,应在HCl气流中低温烘干
(6)氯化铜溶液中加入足量氢氧化钠溶液、过滤得到沉淀为氢氧化铜,沉淀洗涤的操作方法是:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;氢氧化铜加热分解所得黑色固体的质量ng为CuO,根据Cu元素守恒计算CuCl2•xH2O的物质的量,再结合m=nM计算x的值;
解答 解:粗铜中含有Fe,与氯气反应生成CuCl2和FeCl3,为防止水解,应加入过量的稀盐酸进行溶解,并保证金属完全反应,溶液1中的金属离子有Fe3+、Fe2+、Cu2+,加入试剂X目的是将溶液中Fe2+氧化为Fe3+,应为H2O2,还原得到水,是绿色氧化剂,通过调节pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且加入Y可以消耗氢离子且不能引入新杂质,可以为CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3.滤液经过加热浓缩、冷却结晶、过滤、洗涤、干燥得到CuCl2•2H2O.
(1)①Fe2+具有还原性,可以使酸性高锰酸钾溶液褪色,用高锰酸钾溶液可以检验Fe2+,故正确;
②Fe2+能与K3[Fe(CN)6]反应得到蓝色铁氰化亚铁蓝色沉淀,故正确;
③铁离子、铜离子均与NaOH反应生成沉淀,影响亚铁离子检验,故错误;
④铁离子与KSCN反应,溶液呈红色,不能检验Fe2+,故错误;
加入试剂X目的是将溶液中Fe2+氧化为Fe3+,X应为H2O2,还原得到水,是绿色氧化剂,
故答案为:①②;H2O2;
(2)由上述分析可知,试剂X为盐酸,加入过量的盐酸,充分反应,抑制Cu2+水解;
加入Y可以消耗氢离子调节溶液pH,使溶液中Fe3+转化为Fe(OH)3沉淀,过滤分离,且不能引入新杂质,
a.NaOH引入杂质钠离子,故a错误;
b.NH3•H2O 引入铵根离子,故b错误;
c.CuO可以调节PH值,除去杂质,过量的CuO过滤除去,不引入杂质,故c正确;
d.Cu2(OH)2CO3 可以调节PH值,除去杂质,过量的Cu2(OH)2CO3 过滤除去,不引入杂质,故d正确;
e.CuSO4不能调节PH值,引入硫酸根离子,故e错误;
调节pH至4~5之间,使溶液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀;
得到固体2的操作是将不溶固体与液体进行分离,应采取过滤操作,
故答案为:盐酸;充分反应,抑制Cu2+水解;cd;使溶液中Fe3+转化为Fe(OH)3沉淀,Cu2+离子不沉淀;过滤;
(3)B装置中二氧化锰与浓盐酸在加热条件下反应生成氯气,C装置干燥氯气,D装置中粗铜(Fe、Cu的混合物)与氯气反应生成CuCl2和FeCl3,多于的氯气用氢氧化钠溶液吸收,以防污染空气,由于HCl不影响氯气和粗铜的反应的产物,且可以抑制氯化铜水解,氯气中混有的HCl不需要除去.
①仪器A是分液漏斗,故答案为:分液漏斗;
②引发B中反应的操作是:打开分液漏斗上口玻璃塞,旋开分液漏斗活塞,缓慢滴加,并用酒精灯加热B装置;装置B中制取氯气,二氧化锰与浓盐酸发生反应生成氯化锰、氯气、水,反应离子方程式为:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
故答案为:打开分液漏斗上口玻璃塞,旋开分液漏斗活塞,缓慢滴加,并用酒精灯加热B装置;MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(4)①Cu(H2O)42+(aq)+4Cl-(aq)?CuCl42-(aq)+4H2O(l)的平衡常数为K=$\frac{c(CuC{l}_{4}{\;}^{2-})}{c[Cu(H{\;}_{2}O){\;}_{4}{\;}^{2+}]•{c}^{4}(C{l}^{-})}$,
平衡常数只受温度影响,与离子浓度无关,增大氯离子浓度,K值不变,
故答案为:$\frac{c(CuC{l}_{4}{\;}^{2-})}{c[Cu(H{\;}_{2}O){\;}_{4}{\;}^{2+}]•{c}^{4}(C{l}^{-})}$;不变;
②a.将Y稀释,平衡向左反应移动,溶液呈蓝色,可以能够证明CuCl2溶液中转化关系,故a正确;
b.在Y中加入CuCl2晶体,溶液中Cu(H2O)42+浓度增大,平衡向右移动,溶液变为绿色,可以能够证明CuCl2溶液中转化关系,故b正确;
c.在Y中加入NaCl固体,溶液中氯离子浓度增大,平衡向右移动,溶液变为绿色,可以能够证明CuCl2溶液中转化关系,故c正确;
d.取Y进行电解,铜离子放电,溶液颜色最终消失,不能可以能够证明CuCl2溶液中转化关系,故d错误.
故选:abc;
(5)CuCl2•xH2O晶体加热容易分解,且氯化铜易水解,应在HCl气流中低温烘干,故答案为:D;
(6)氯化铜溶液中加入足量氢氧化钠溶液、过滤得到沉淀为氢氧化铜,沉淀洗涤的操作方法是:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;
氢氧化铜加热分解所得黑色固体的质量ng为CuO,根据Cu元素守恒:n(CuCl2•xH2O)=n(CuO)=$\frac{n}{80}$mol,则$\frac{n}{80}$mol×(135+18x)=mg,解得x=$\frac{80m-135n}{18n}$,
故答案为:向过滤器中加入水至完全浸没沉淀,过滤,重复2~3次;$\frac{80m-135n}{18n}$.
点评 本题考查化学工艺流程及实验制备,涉及对实验装置与操作及试剂的分析评价、物质分离提纯、化学平衡移动、化学计算等,要求学生具备扎实的基础与综合运用能力,难度很大.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
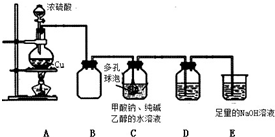
| 假 设 | 操作 | 现 象 | 原理 |
| Na2S2O4 为强 碱弱酸盐,其溶 液为碱性. | 取少量溶液于试管中,滴加 紫色石蕊试液 | 溶液变 成蓝色 | S2O42-水解,使溶液成碱性 |
| Na2S2O4 中 S 为 +3 价,具有较强 的还原性. | 取少量溶液于试管中,滴加过量新制氯水,再 滴加 BaCl2 溶液 | 有白色沉淀生 成 | 该反应的离子方程式依次为: 4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+ Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com