
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 |
| n |
| V |
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 | ②⑦⑧⑨ | ④ | ③⑤⑥⑨ |
| 34.2g |
| 342g/mol |
| 0.3mol |
| 0.25L |
| 5.4g |
| 27g/mol |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
| A、Na2CO3是钠盐 |
| B、Na2CO3是盐 |
| C、Na2CO3是碱 |
| D、Na2CO3是碳酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入Na2CO3溶液 |
| B、向水中加入Al2(SO4)3固体 |
| C、向水中加入NaHSO4溶液 |
| D、将水加热到100℃,使pH=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
B、 32gS8单质中含有的S-S键个数为NA(见图) |
| C、10L 0.1mol/L Na2S的水溶液中,S2-、HS-两种微粒数之和为NA个 |
| D、标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清的石灰水跟盐酸反应:H++OH-═H2O |
| B、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| D、金属钠跟水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应Ca2++CO32-=CaCO3↓. |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
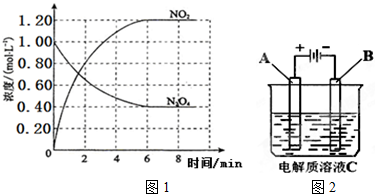
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com