
| 10g |
| 60g/mol |
| 1 |
| 6 |
| 425 |
| 8075 |
| 425 |
| 8075 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
| A、14 | B、38 | C、57 | D、无定值 |
查看答案和解析>>
科目:高中化学 来源: 题型:
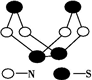 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )| A、该物质的摩尔质量为46 g?mol-1 |
| B、1 mol该物质含有9个共价键 |
| C、相同质量的该物质和S2N2所含原子个数之比为1:1 |
| D、该物质与S2N2互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
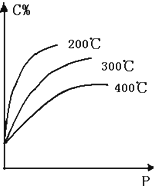 对于反应mA(s)+nB(g)?eC(g)+f D(g),当其它条件不变,平衡时C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是( )
对于反应mA(s)+nB(g)?eC(g)+f D(g),当其它条件不变,平衡时C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是( )| A、化学方程式中n<e+f |
| B、达到平衡后,加入催化剂,则C%增大 |
| C、达到平衡后,若升温,平衡逆向移动 |
| D、达到平衡后,增加A的量,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 | 相对分子质量 | 密度/g?cm-3[来源:.Com] | 沸点 | 水中溶解性 | |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 | |
| 环己醇 | 100 | 0.982 | 160.8 | 微溶 | |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氧化 |
| Ag(NH3)2OH |
| H+ |
| CH3OHH+ |
| △ |
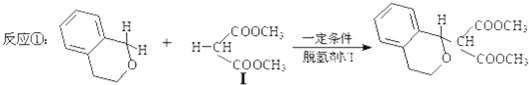
 )分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为
)分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为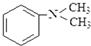 与1分子
与1分子 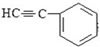 在一定条件下可发生类似反应①的反应,其产物分子的结构简式为
在一定条件下可发生类似反应①的反应,其产物分子的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

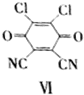
| A、Ⅰ在空气中能稳定存在 |
| B、Ⅱ中所有原子均有可能共面 |
| C、可用FeCl3溶液鉴别有机物Ⅱ和Ⅲ |
| D、1mol产物III与足量溴水反应,消耗Br2的物质的量为1.5mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com