
| A. | 碱性氧化物 氧化铁 FeO | B. | 酸性氧化物 碳酸气 CO2 | ||
| C. | 酸 硫酸 H2S | D. | 盐 纯碱 NaOH |
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、HCO3-、Ca2+ | B. | Ba2+、H+、Cl- | C. | Ca2+、NH4+、HCO3- | D. | Mg2+、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键没有方向性和饱和性,而共价键有方向性和饱和性 | |
| B. | 离子键的强弱主要决定于离子半径和离子所带电荷数 | |
| C. | 配位键在形成时,由成键双方各提供一个电子形成一对共用电子 | |
| D. | 金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜跟硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 硫酸与氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 小苏打投入过量的澄清石灰水中 HCO3-+Ca2++OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
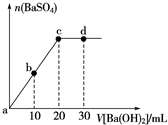
| A. | 溶液的pH:a<b<c<d | B. | 溶液的导电性:c<d | ||
| C. | a、b溶液呈酸性 | D. | c、d溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Fe2+、NO3-、Na+、SO42- | |
| B. | 水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Ⅱ表示的是滴定醋酸的曲线 | |
| B. | V(NaOH)=20ml时,${C_{(C{l^-})}}$=${C_{(C{H_3}CO{O^-})}}$ | |
| C. | PH=7时,滴定醋酸消耗V(NaOH)小于20ml | |
| D. | V(NaOH)=10ml时,醋酸溶液中:${C_{(N{a^+})}}$>${C_{(C{H_3}CO{O^-})}}$>${C_{({H^+})}}$>${C_{(O{H^-})}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 CsCl CBr4 CF4 | B. | SiO2 CsCl CF4 CBr4 | ||
| C. | CsCl SiO2 CBr4 CF4 | D. | CF4 CBr4 CsCl SiO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com