
 的路线如下图所示.
的路线如下图所示.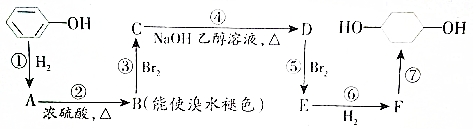
 ,F
,F .
. .
. .
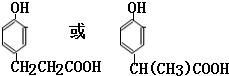
. 分析 根据苯酚的性质可知,与氢气发生加成反应生成A为 ,
, 在浓硫酸作用下发生消去反应生成B为
在浓硫酸作用下发生消去反应生成B为 ,进而与溴发生加成反应生成C为
,进而与溴发生加成反应生成C为 ,C在NaOH乙醇溶液的作用下发生消去反应生成D为
,C在NaOH乙醇溶液的作用下发生消去反应生成D为 ,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由
,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由 可知应为1,4加成产物,则E为
可知应为1,4加成产物,则E为 ,F为
,F为 ,F最后水解可生成
,F最后水解可生成 ,结合有机物的结构和性质解答该题.
,结合有机物的结构和性质解答该题.
解答 解:根据苯酚的性质可知,与氢气发生加成反应生成A为 ,
, 在浓硫酸作用下发生消去反应生成B为
在浓硫酸作用下发生消去反应生成B为 ,进而与溴发生加成反应生成C为
,进而与溴发生加成反应生成C为 ,C在NaOH乙醇溶液的作用下发生消去反应生成D为
,C在NaOH乙醇溶液的作用下发生消去反应生成D为 ,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由
,D与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,由 可知应为1,4加成产物,则E为
可知应为1,4加成产物,则E为 ,F为
,F为 ,F最后水解可生成
,F最后水解可生成 ,
,
(1)根据分析可知B的结构简式为 ,F的结构简式为
,F的结构简式为 ,
,
故答案为: ;
; ;
;
(2)反应②为 在浓硫酸作用下发生消去反应生成
在浓硫酸作用下发生消去反应生成 ,该反应为消去反应,
,该反应为消去反应,
故答案为:消去反应;
(3)反应④为 在NaOH乙醇溶液的作用下发生消去反应生成
在NaOH乙醇溶液的作用下发生消去反应生成 ,反应的化学方程式为:
,反应的化学方程式为: ,
,
故答案为: ;
;
(3)D为 ,与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,则对应的副产品为:
,与溴可发生1,2加成或1,4加成,或全部发生加成反应生成四溴产物,则对应的副产品为: ,
,
故答案为: .
.
点评 本题考查有机物的推断,题目难度中等,解答本题的关键是根据苯酚能发生加成反应的性质进行推断,注意掌握常见有机物结构与性质,试题培养了学生的分析能力及逻辑推理能力.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在钠、钾、铷三种单质中,钠的熔点最高 | |
| B. | 所有碱金属均为银白色 | |
| C. | 同一主族卤素单质从上到下熔沸点依次升高 | |
| D. | 液溴易挥发,可以通过水封的方式进行保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
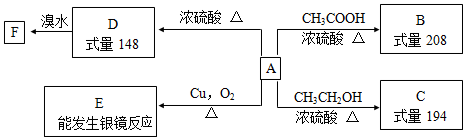
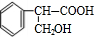 ;E中所含官能团的名称为醛基、羧基.
;E中所含官能团的名称为醛基、羧基.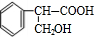 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$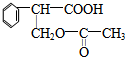 +H2O.
+H2O.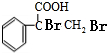 .
. .(写出一种即可)
.(写出一种即可)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
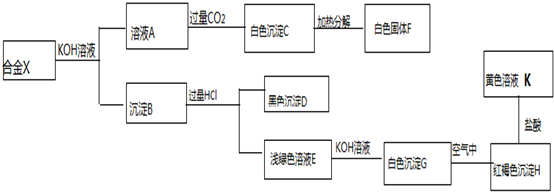
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
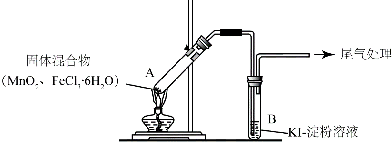
| 操作 | 现象 |
| 点燃酒精灯,加热 | iA中部分固体溶解,上方出现白雾 ii稍后,产生黄色气体,管壁附着黄色液滴 iiiB中溶液变蓝 |
| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈浅橙色;未检出Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应速率等于逆反应速率 | B. | 反应物和生成物浓度不再发生变化 | ||
| C. | 反应体系中混合物的组成保持不变 | D. | 正、逆反应速率都为零 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com