

 4CO(g)+BaS(s)△H1=+571.2kJ?mol-1 ①
4CO(g)+BaS(s)△H1=+571.2kJ?mol-1 ① 2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1 ②
2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1 ② 2CO(g)的△H= 。
2CO(g)的△H= 。



科目:高中化学 来源:不详 题型:单选题
| A.把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-= 2HClO+CaSO3↓ |
| B.足量铁屑溶于稀硫酸:2Fe+6H+=2Fe3++3H2↑ |
| C.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
| D.铝片溶于烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHSO3溶液中投入过氧化钠粉末:4HSO3- +2Na2O2 = 4SO32- + O2↑ + 4Na+ |
| B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O==AlO2-+4NH4++2H2O |
| C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| D.将1 mol/L NaAlO2溶液和1.5 mol/L HCl溶液等体积互相均匀混合: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.足量的硫酸铝溶液与纯碱溶液反应: 2A13++3CO32-+3H20 =2A1(OH)3↓+3CO2↑ |
B.NaHS溶液的水解方程式: HS-+H2O H3O++S2- H3O++S2- |
| C.Fe(OH)3与足量的HI溶液反应: Fe(OH)3+3H+=Fe3++3H2O |
| D.向亚硫酸氢铵溶液中加入足量的NaOH溶液: NH4++OH-=NH3·H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Ca(OH) 2与少量的NaHCO3 | B.Ca(OH) 2与少量的Ca(HCO3) 2 |
| C.Ca(HCO3) 2与足量的NaOH | D.Ca(OH) 2与足量的Ca(HCO3) 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32-+2H+= CO2↑+ H2O |
B.向苯酚钠溶液中通入少量的CO2: + CO2 +H2O→ + CO2 +H2O→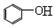 + HCO3- + HCO3- |
| C.足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++2H2O+NO↑ |
| D.向漂白粉溶液中通入少量二氧化硫: Ca2+ +2ClO- + SO2+H2O=CaSO3↓+ 2HClO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用氢氧化钠溶液除去铝片表而上的氧化膜:Al3++4OH-=AlO2-+2H2O |
| B.在含3.2amolHNO3的稀溶液中,加入amol铁粉:5Fe+4NO3-+16H+=3Fe2++2Fe3++4NO↑+8H2O |
| C.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D.过氧化氢能使酸性KMnO4溶液褪色:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2 = NO+2NO↑+H2O |
B.NH4HCO3溶液与足量KOH浓溶液共热:NH+OH-  NH3↑+H2O NH3↑+H2O |
| C.铁溶于足量的稀硝酸,溶液变黄:3Fe+8H++2NO= 3Fe2++2NO↑+4H2O |
| D.NaHSO4溶液与NaOH溶液混合:OH-+H+= H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.小苏打与氢氧化钠溶液的反应:OH-+ H+ = H2O |
| B.实验室制二氧化碳:CaCO3 + 2H+ = CO2↑ + H2O + Ca2+ |
| C.氯气与水反应:Cl2 + H2O = Cl-+ ClO-+ 2H+ |
| D.AlCl3溶液与过量氨水反应:Al3+ + 4NH3·H2O = AlO2-+ 4NH4+ + 2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com