
下列说法中正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.熵增加且放热的反应一定是自发反应
D.非自发反应在任何条件下都不能实现
科目:高中化学 来源: 题型:
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2 NH3(g)+CO2(g)  NH2COONH4(s) + Q (Q > 0 )
NH2COONH4(s) + Q (Q > 0 )
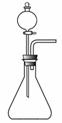
如用右图装置制取氨气,你所选择的试剂是 。
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化
碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
发生器用冰水冷却的原因是___________ __ _。
液体石蜡鼓泡瓶的作用是__________________________________________________。
从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a. 常压加热烘干 b. 高压加热烘干 c. 真空40 ℃以下烘干
 尾气处理装置如右图所示。双通玻璃管的作用:________ ;
尾气处理装置如右图所示。双通玻璃管的作用:________ ;
浓硫酸的作用: 、______________、 _。
取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水
充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量
为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
(精确到2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关工业生产的叙述正确的是
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高SO2转化为SO3的转化率
C.电解精炼铜时,精铜作阴极
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2 NH3(g)+CO2(g)  NH2COONH4(s) + Q (Q > 0 )
NH2COONH4(s) + Q (Q > 0 )
如用右图装置制取氨气,你所选择的试剂是 。
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化
碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
发生器用冰水冷却的原因是___________ __ _。
液体石蜡鼓泡瓶的作用是__________________________________________________。
从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a. 常压加热烘干 b. 高压加热烘干 c. 真空40 ℃以下烘干
 尾气处理装置如右图所示。双通玻璃管的作用:________ ;
尾气处理装置如右图所示。双通玻璃管的作用:________ ;
浓硫酸的作用: 、______________、 _。
取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水
充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量
为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
(精确到2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是
A. FeS不溶于水,但能溶于稀盐酸中 B.钢铁在潮湿的空气中容易生锈
C.实验室中常用排饱和食盐水的方式收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:

下列叙述不正确的是
A. 放电时负极反应为:Zn - 2e— + 2OH— == Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3 -3e— + 5OH— == FeO42— + 4H2O
C. 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。 滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
 (2)滴定时边滴边摇动锥形瓶,眼睛应观察
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是
由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)右图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度: mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中正确的是
A.CS2为V形分子
B.NCl3的空间构型为平面三角形
C.铝的第一电离能比镁的第一电离能大
D.SiF4和H2O的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色 | 含有Fe2+溶液 |
| B | 向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 含有CO32-溶液 |
| C | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 | 可能为Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊。 | 可能为Ca(OH)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com