
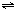 Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深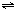 Fe(SCN)3反应达平衡时,增加KSCN的浓度,则平衡向着正方向进行,产物浓度增大,体系颜色变深,能用勒夏特利原理来解释,故D不选.
Fe(SCN)3反应达平衡时,增加KSCN的浓度,则平衡向着正方向进行,产物浓度增大,体系颜色变深,能用勒夏特利原理来解释,故D不选.

科目:高中化学 来源: 题型:
| A、在硫化氢水溶液中加入碱有利于S2-的生成 | B、热的纯碱溶液去污能力强 | C、高压有利于合成氨反应 | D、500℃左右比室温更利于合成氨反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com