
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
A.标准状况下,2.24 L Cl2与足量的稀NaOH溶液反应,转移电子总数为0.2NA
B.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
C.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中
D.标准状况下,0.1NA的SO3的体积约为2.24 L
科目:高中化学 来源:2016届河南省高三上学期第八次大考化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲 + 乙 = 丁 + 己,甲 + 丙 = 戊 + 己;0.1 mol·L-1丁溶液的pH为13(25℃)。下列说法正确的是
A.1 mol甲与足量的乙完全反应共转移了1 mol电子
B.Y元素在周期表中的位置为第三周期第ⅣA族
C.原子半径:W>Z>Y>X
D.1.0 L 0.1 mol·L-1戊溶液中阴离子总的物质的量小于0.1 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
常温下,在下列溶液中发生如下反应:
①16H++10Z-+2XO4-=2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-由此判断下列说法正确的是
A.反应Z2+2A2+===2A3++2Z-不能进行
B.Z元素在①③反应中均被氧化
C.氧化性由弱到强的顺序是XO、Z2、B2、A3+
D.还原性由强到弱的顺序是A2+、B-、Z-、X2+
查看答案和解析>>
科目:高中化学 来源:2016届北京市朝阳区高三上学期期中统考化学试卷(解析版) 题型:选择题
将CO2转化为 CH4,既可以减少温室气体的排放,又能得到清洁能源。已知:
CO2(g)+2H2O(g) CH4(g)+2O2(g) ΔH= +802 kJ·mol-1
CH4(g)+2O2(g) ΔH= +802 kJ·mol-1
右图为在恒温、光照和不同 催化剂(Ⅰ、Ⅱ)作用下,体积为1 L的密闭容器中n (CH4)随光照时间的变化曲线。下列说法正确的是
催化剂(Ⅰ、Ⅱ)作用下,体积为1 L的密闭容器中n (CH4)随光照时间的变化曲线。下列说法正确的是

A.0~25h内,催化剂Ⅰ的催化效果比催化剂Ⅱ的效果好
B.0~16h内,v(H2O)Ⅰ = 1.5 mol/(L·h)
C.在两种不同催化剂下,该反应的平衡常数不相等
D.反应开始后的15h内,第Ⅰ种催化剂的作用下,得到的CH4最多
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次联考化学试卷(解析版) 题型:选择题
用NA表示的值,下列说法正确的是
A.24.5L氢气中所含氢原子数一定大于2NA
B.lmolCH3+电子数为9NA
C.l00g 60%CH3COOH水溶液中含有的分子数为NA
D.常温常压下0.lmol CO和NO的混合气体含氧原子数为0.lNA
查看答案和解析>>
科目:高中化学 来源:2016届山东省德州市高三上学期期中测试化学试卷(解析版) 题型:填空题
铜及其化合物在生产、生活中应用广泛。回答下列问题:
(1)用新制Cu(OH)2与葡萄糖反应可制备Cu2O,该反应中葡萄糖是 (填“氧化剂”或“还原剂”)。
(2)用H2O2、H2SO4混合溶液浸泡废印刷电路板可制备CuSO4以实现铜的回收利用,其离子方程式为 。
(3)用NH4NO3氧化海绵铜(含Cu的CuO)生产CuCl的部分流程如下:
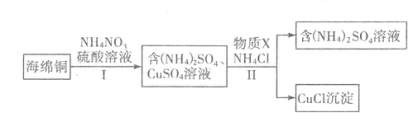
①步骤I中反应温度不宜过高的原因是 ,当0.5 mol NH4NO3参加反应时,反应中有4 mol电子发生转移,则铜参加反应的离子方程式为 。
②步骤Ⅱ中物质X可选用 (填字母),该物质需过量的原因,其一是加快反应速率,其二是 。
a.Cu b.Cl2 c.H2O2 d.(NH4)2SO3
查看答案和解析>>
科目:高中化学 来源:2016届山西省晋中市四校高三上学期期中联考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 (s) + 2Fe3+(aq) = 2Fe(OH)3 (s) + 3Mg2+(aq)
B.钠与CuSO4溶液反应:2Na + Cu2+ = Cu↓ + 2Na+
C.已知:酸的强弱H2CO3>HClO>HCO3-,则:2ClO-+ CO2(少量) + H2O=CO32-+ 2HClO
D.将足量的NaHCO3溶液加入少量澄清石灰水中:Ca2+ + OH- + HCO3-=CaCO3↓ + H2O
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中模块测试化学试卷(解析版) 题型:选择题
近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu20+H2O= 2Cu十2Li++20H-,下列说法不正确的是

A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,负极的电极反应式为Cu20+H2O+2e-=Cu+2OH-
C.通空气时,铜被腐蚀,表面产生Cu20
D.整个反应过程中,铜相当于催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com