
自然界矿物重晶石的主要成分是硫酸钡,它不溶于水,也不溶于任何一种酸和碱,纯净的硫酸钡可供医疗等方面应用.某课外活动小组的同学用重晶石矿和焦炭为原料制取纯净的硫酸钡,部分流程如图所示(假设矿物中杂质不与焦炭反应):请按要求填空:
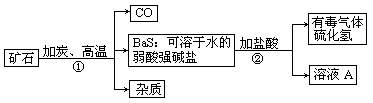
(1)在步骤①中化合价升高的元素为________,化合价降低的元素为________;溶液A的溶质的化学式为________.
(2)写出用溶液A制取Ba(OH)2的化学方程式:________.
(3)某同学指出:上述步骤②产生了有毒气体硫化氢,应将方法改进.请你给出改进意见,使该实验不产生硫化氢气体,又能获得纯净的硫酸钡,并请写出有关的化学方程式:________.
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
时间(h) 溶出率 温度 |
1.5 | 2.5 | 3.0 | 3.5 | 4.0 | 5.0 |
| 800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 | 0.183 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 | 0.687 |
| 860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 | 0.690 |
| 950℃ | 0.669 | 0.714 | 0.710 | 0.714 | 0.714 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:022
自然界矿物质财富重晶石的主要成分是硫酸钡,它不溶于水,也不溶于任何一种酸和碱,纯净的硫酸钡可供医疗等方面应用。某课外活动小组的同学用重晶石矿和焦炭为原料制取纯净的硫酸钡,部分流程如框图所示(假设矿物中杂质不与焦炭反应):
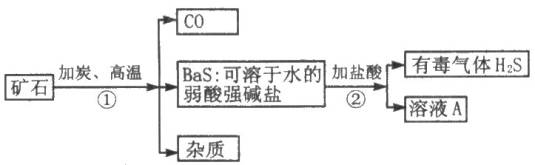
请按要求填空:
⑴在步骤①中化合价升高的元素为 ,化合价降低的元素为 ,溶液A的溶质的化学式为 。
⑵用溶液A制取Ba(OH)2的化学方程式为 。
⑶某同学指出:上述步骤②产生了有毒气体硫化氢,应将方法改进。请你写出改进意见,使该实验不产生硫化氢气体,又能获得纯净的硫酸钡,并请写出有关的化学方程式
。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022

请按要求填空:
⑴在步骤①中化合价升高的元素为 ,化合价降低的元素为 ,溶液A的溶质的化学式为 。
⑵用溶液A制取Ba(OH)2的化学方程式为 。
⑶某同学指出:上述步骤②产生了有毒气体硫化氢,应将方法改进。请你写出改进意见,使该实验不产生硫化氢气体,又能获得纯净的硫酸钡,并请写出有关的化学方程式
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com