
| A.将①与②分别稀释相同倍数后溶液的pH:①>② |
| B.若②与③混合后溶液呈中性,则在常温下Ka(CH3COOH)=Kb(NH3?H2O) |
| C.③与④中已电离的水分子的数目相等 |
| D.②与④混合所得溶液显酸性,则:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |


科目:高中化学 来源:不详 题型:单选题
| A.溶液的体积:10V甲≤V乙 |
| B.水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D.若分别与5mlpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

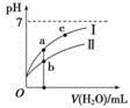
| A.水电离出的氢离子浓度:a>b |
| B.c点时恰好中和 |
| C.在d~e之间存在如下关系:C(Na十)>c(CH3COO-)>c(H十)>c(OH一) |
| D.e点时溶液中溶质是CH3COONa和CH3COOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,某溶液中由水电离出来的c(H+)=1×10―amol·L―1,若a<7,则该溶液可能为NaHSO4溶液 |
| B.中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸) >V(醋酸) |
| C.pH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| D.已知Ag2CrO4的Ksp为1.12×10-12,将等体积的1×10-4mol·L-1的AgNO3溶液和1×10-4mol·L-1K2CrO4溶液混合,会有Ag2CrO4沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.白醋中滴入石蕊试液呈红色 | B.白醋加入豆浆中有沉淀产生 |
| C.蛋壳浸泡在白醋中有气体放出 | D.pH试纸显示醋酸的pH为2~3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c (Ac-)>c (Cl-)>c (H+)> c (HAc) | B.c (Na+)+c (H+)=c (Ac-)+c (Cl-) |
| C.c (Ac-)=c (Cl-)>c (H+)>c (HAc) | D.c (Ac-)>c (Cl-)>c (HAc)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、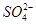 |
B.加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的溶液:Al3+、Ba2+、Cl-、 |
C.水电离产生的c(H+)=10-13mol·L-1的溶液中:Na+、Cl-、 、 、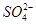 |
D.0.1 mol·L-1HNO3溶液中:Mg2+、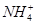 、Fe2+、Cl- 、Fe2+、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
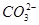
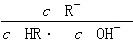 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com