|
|
|
常温下,将20.0 g质量分数为14.0%的KNO3溶液与30.0 g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15 g/cm3的混合溶液.
计算:
(1)混合后溶液的质量分数.
(2)混合后溶液的物质的量浓度(保留至小数点后两位数字).
(3)在1000 g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?(保留至小数点后两位数字)
|
|
|
练习册系列答案
相关习题
科目:高中化学
来源:人民教育出版社 高三年级(选修)第三册
题型:
|
|
|
下列判断正确的是
①Ca(OH)2微溶于水,所以Ca(OH)2是弱电解质;
②强电解质溶液的导电能力可能比弱电解质导电能力弱;
③液态氯化氢不导电,但它是电解质;
④碳酸氢钠是弱酸的酸式盐,所以是弱电解质;
⑤SO3溶于水后导电,所以SO3是电解质;
⑥Cu能导电,但它不是化合物,所以Cu是非电解质
|
| [ ] |
A. |
②③
|
B. |
②③⑥
|
C. |
①④⑤⑥
|
D. |
②③⑤
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
标准状况下,32 g某气体的分子数与22 g CO2的分子数相同,该气体的摩尔质量为
|
| [ ] |
A. |
32
|
B. |
32 g·mol-1
|
C. |
64 g·mol-1
|
D. |
64
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
下列每组分别给出了两个量,其中可以组成一个物质的量的公式的组有

|
| [ ] |
A. |
①②⑤
|
B. |
②③④
|
C. |
①④⑤
|
D. |
①③
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
已知某KOH样品中含水7.62%,含K2CO3 2.23%,含KOH 90%.现将1.00 g样品加入60.0 mL 1.00 mol/L的盐酸中,过量的酸用1.070 mol/L KOH溶液中和.蒸发溶液,蒸发到无水时,可得的固体的质量为
|
| [ ] |
A. |
3.00 g
|
B. |
3.43 g
|
C. |
4.50 g
|
D. |
无法计算
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
下列有关说法中正确的是
|
| [ ] |
A. |
有单质生成的反应一定是置换反应
|
B. |
焰色反应是元素表现出来的化学性质
|
C. |
由两种元素组成,原子个数比为1∶1的物质一定是纯净物
|
D. |
能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
将标准状况下的V L HCl(气)溶于1000 g水中,得到的盐酸密度为r
g/cm3,则该盐酸的物质的量浓度为
|
| [ ] |
A. |
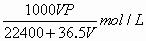
|
B. |
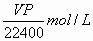
|
C. |
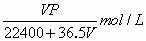
|
D. |
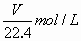
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本概念
题型:
|
|
|
肼(N2H4)通常作为火箭的燃料.已知3.2 g液态肼在O2(g)中完全燃烧,生成N2(g)和H2O(l),放出62.2kJ热量,写出上述反应的热化学方程式是________.
|
|
|
查看答案和解析>>
科目:高中化学
来源:人民教育出版社 基本理论
题型:
|
|
|
实验室用足量铁粉与一定量的某浓度的盐酸反应来制得氢气.由于反应速率太快,不易操作.为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
|
| [ ] |
A. |
CH3COONa固体
|
B. |
NaOH溶液
|
C. |
(NH4)2SO4粉末
|
D. |
K2SO4固体
|
|
|
查看答案和解析>>

 名校课堂系列答案
名校课堂系列答案