
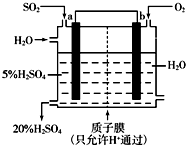
 在硫酸工业中,SO2转化为SO3是一个关键步骤
在硫酸工业中,SO2转化为SO3是一个关键步骤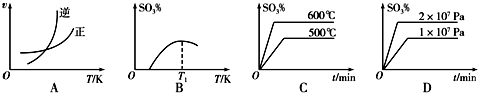
分析 (1)SO2气体通入酸性KMnO4中,酸性KMnO4褪色,高锰酸钾中锰元素是最高价具有氧化性,二氧化硫具有还原性;Mn元素化合价由+7价降低到+2价,化合价变化5价,S元素化合价由+4价升高到+6价,化合价变化2价,氧化还原反应中氧化剂和还原剂得失电子数目相等;
(2)根据方程式的热量计算参加反二氧化硫物质的量,计算平衡时各物质的浓度,代入平衡常数表达式K=$\frac{c(S{O}_{3})}{c(S{O}_{2})×{c}^{\frac{1}{2}}({O}_{2})}$计算;
(3)A.升高温度,平衡逆向移动;
B.升高温度,平衡逆向移动,三氧化硫的含量降低;
C.升高温度,加快反应速率到达平均的时间缩短,逆反应速率增大更多,平衡向逆反应方向移动,三氧化硫的含量降低;
D.增大压强,加快反应速率到达平均的时间缩短,平衡向正反应方向移动,三氧化硫的含量增大;
(4)SO2、O2、SO3气体平衡浓度都比原来增大,如体积不变,则各种物质的物质的量都增大,如体积变化,各种物质的浓度都增大,则应缩小体积;
(5)原电池负极发生氧化反应,SO2被氧化生成SO42-;钡离子和硫酸根离子生成硫酸钡白色沉淀,据此检验硫酸根离子.
解答 解:(1)SO2气体通入酸性KMnO4中,酸性KMnO4褪色,高锰酸钾中锰元素是最高价具有氧化性,二氧化硫具有还原性;Mn元素化合价由+7价降低到+2价,化合价变化5价,S元素化合价由+4价升高到+6价,化合价变化2价,氧化还原反应中氧化剂和还原剂得失电子数目相等,则氧化剂和还原剂物质的量之比为2:5,
故答案:还原;2:5;
(2)在100L的密闭容器中加入4.0mol SO2(g)和10.0molO2(g),当反应达到平衡时共放出热量196kJ,则消耗SO2 为$\frac{196kJ}{98kJ/mol}$=2mol,
SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)
起始mol):4.0 10.0 0
转化(mol):2.0 1.0 2
平衡(mol):2.0 9.0 2
则平衡时,c(SO2)=0.02mol/L,c(O2)=0.09mol/L,c(SO3)=0.02mol/L,
平衡常数K=$\frac{c(S{O}_{3})}{c(S{O}_{2})×{c}^{\frac{1}{2}}({O}_{2})}$=$\frac{0.02}{0.02×\sqrt{0.09}}$3.33,
故答案为:K=$\frac{c(S{O}_{3})}{c(S{O}_{2})×{c}^{\frac{1}{2}}({O}_{2})}$=3.33;
(3)A.升高温度,逆反应速率增大更多,平衡向逆反应方向移动,图象与实际符合,故A正确;
B.升高温度,平衡向逆反应方向移动,三氧化硫的含量降低,图象与实际符合,故B正确;
C.升高温度,加快反应速率到达平均的时间缩短,平衡向逆反应方向移动,三氧化硫的含量降低,图象与实际不符,故C错误;
D.增大压强,加快反应速率到达平均的时间缩短,正反应速率增大更多,平衡向正反应方向移动,三氧化硫的含量增大,图象与实际符合,故D正确;
故答案为:C;
(4)A.保持温度和容器体积不变,充入2mol SO3,平衡向逆反应分析移动,则SO2、O2、SO3气体平衡浓度都比原来增大,故A正确;
B.保持温度和容器体积不变,充入2mol N2,对平衡移动没有影响,各物质的浓度不变,故B错误;
C.保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2,平衡向正反应方向移动,则SO2、O2、SO3气体平衡浓度都比原来增大,故C正确;
D.升高温度,平衡向逆反应方向移动,SO3的浓度减小,故D错误;
E.移动活塞压缩气体,体积减小,各物质的浓度都增大,故E正确.
故答案为:ACE;
(5)依据图装置分析,二氧化硫失电子发生氧化反应,二氧化硫被氧化为三氧化硫溶于水生成硫酸,电极反应为:SO2+2H2O-2e-=SO42-+4H+;
检验硫酸根离子的方法为:取少量溶液于试管中加入盐酸,无明显现象,再加入BaCl2溶液,若产生白色沉淀说明溶液中含SO42-,
故答案为:SO2+2H2O-2e-=SO42-+4H+;取少量溶液于试管中加入盐酸,无明显现象,再加入BaCl2溶液,若产生白色沉淀说明溶液中含SO42-.
点评 本题考查化学平衡常数的有关计算、影响化学平衡的因素、化学平衡图象、电解原理、氧化还原反应等,侧重于学生的分析能力和计算能力的考查,题目难度中等,试题是对学生综合能力的考查,注意基础知识的理解掌握.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
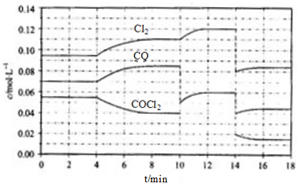 COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g)△H=+108kJ•mol-1.反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图(第10min到14min的COCl2浓度变化曲线未示出):
COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g)△H=+108kJ•mol-1.反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图(第10min到14min的COCl2浓度变化曲线未示出):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用物质A表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质A的转化率为70% | |
| D. | 2 s 时物质B的浓度为 0.7 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
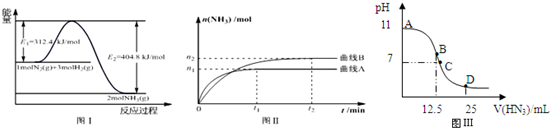
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磷(P)基态原子最外层轨道表示式: | |
| B. | 钢铁发生吸氧腐蚀的正极反应式: O2+4H++4e-═2H2O | |
| C. | 葡萄糖的实验式:C6H12O6 | |
| D. | 氰基的电子式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com