
| A.NH4+、K+、OH-、SO42- | B.Na+、Fe2+、NO3-、Cl- |
| C.Ca2+、Cl-、HCO3-、K+ | D.K+、Na+、Br-、SO42- |
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:不详 题型:填空题


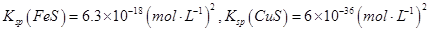
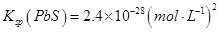
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
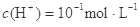 时,有气体产生:而当溶液中
时,有气体产生:而当溶液中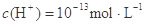 时,又能生成沉淀,则该组离子可能是( )
时,又能生成沉淀,则该组离子可能是( )| A.Na+、Ba2+、NO3-、CO32- | B.Ba2+、K+、Cl—、NO3- |
| C.Mg2+、NH4+、SO42-、Cl- | D.Fe2+、Na+、SO42-、NO3— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验事实 | 结论或解释 |
| A | 将40 g NaOH溶于1 L蒸馏水中 | 该溶液的物质的量浓度为1mol﹒L-1 |
| B | 0.1 mol/L CH3COOH溶液在稀释过程中 | 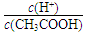 将变小 将变小 |
| C | 酸H2X为弱酸 | 常温下,盐NaHX溶液pH一定大于7 |
| D | 在溶液的稀释过程中 | 离子浓度:有的可能增大,有的可能减小,有的可能不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Br-、CO32- | B.Na+、SO32-、I- |
| C.Ca2+、I-、SO32- | D.Ca2+、CO32-、Br- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2S溶液中: SO42-、K+、ClO-、Cu2+ |
| B.新制氯水中: Cl-、NO3-、Na+、SO32- |
| C.0.1 mol·L-1的NaOH溶液 中:K+、Na+、SO42-、CO32- |
| D.由水电离出的c(OH-)=1×10-11 mol/L的溶液中:K+、Al3+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com