

分析 (1)根据二氧化碳的质量,利用反应的化学方程式可计算碳酸钠的质量;
(2)根据生成的氯化钠的质量和在溶液中的质量分数,求出所得氯化钠溶液的质量,然后求出盐酸溶液的质量,继而求出盐酸的质量分数.
解答 解:设恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量为x,碳酸钠完全反应生成氯化钠的质量为y,消耗稀盐酸的溶质质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
则有:$\frac{106}{X}=\frac{73}{Z}=\frac{117}{y}=\frac{44}{4.4}$
解得:x=10.6g
z=7.3g
y=11.7g
若恰好完全反应时所得溶液的质量为$\frac{11.7g}{5%}$=234g
稀盐酸的溶夜质量=234g+4.4g-138.4g=100g
则稀盐酸的溶质质量分数是$\frac{7.3g}{100g}×$ 100%=7.3%
(1)答:恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量是10.6g
(2)答:稀盐酸的溶质质量分数是7.3%.
点评 本题主要考查化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.本题较复杂,计算的知识点多,学生利用图象分析出二氧化碳的质量代入化学反应方程式计算是解答的突破口.


科目:高中化学 来源: 题型:选择题
| A. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═2Fe2++Fe3++4H2O | |
| B. | FeCl3溶液腐蚀铜线路板:Fe3++Cu=Cu2++Fe2+ | |
| C. | 金属铝加入到NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键是相邻原子间的相互作用 | |
| B. | 化学键既存在于相邻原子之间,又存在与相邻分子之间 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈互吸引作用 | |
| D. | 化学键通常是指物质中相邻的原子或离子之间存在的强烈相互作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子的质量几乎全部集中在原子核上 | |
| B. | 放射性同位素可以用于食物保鲜和肿瘤的治疗 | |
| C. | 在含有多个电子的原子里能量高的电子在离核较近的区域内运动 | |
| D. | ${\;}_{92}^{234}$、${\;}_{92}^{235}$U、${\;}_{92}^{238}$U三种核素互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol•L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应::Ca2++CO32-=CaCO3↓(写离子方程式) |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol•L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4(或HNO3、H2CO3) | ③NaOH(或KOH) ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO4(或K2CO3、Na2SO3) | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
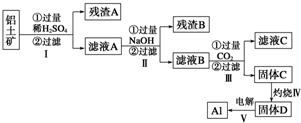
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验目的 | 实验设计 |
| A | 除去CO2中少量的SO2 | 将混合气体通过饱和Na2CO3溶液 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸 |
| C | 证明H2CO3酸性比苯酚强 | 将CO2通入苯酚钠溶液中 |
| D | 检验溶液中是否含有Fe2+ | 向溶液中滴入氯水水后,再滴加KSCN 溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com