
| A. | IBr的化学性质不如氯气活泼 | |
| B. | 在很多反应中IBr充当氧化剂 | |
| C. | IBr跟水反应时既是氧化剂又是还原剂 | |
| D. | 跟NaOH溶液反应生成NaBr和NaIO |
科目:高中化学 来源: 题型:选择题
 用Pt电极电解含有Ag+、Cu2+和X3+各0.1mol的溶液,阴极析出固体物质的质量m(g)与回路中通过电子的物质的量n(mol)的关系如图所示.则下列氧化性强弱的判断正确的是( )
用Pt电极电解含有Ag+、Cu2+和X3+各0.1mol的溶液,阴极析出固体物质的质量m(g)与回路中通过电子的物质的量n(mol)的关系如图所示.则下列氧化性强弱的判断正确的是( )| A. | Ag+>X3+>Cu2+>H+>X2+ | B. | Ag+>Cu2+>X3+>H+>X2+ | ||
| C. | Cu2+>X3+>Ag+>X2+>H+ | D. | Cu2+>Ag+>X3+>H+>X2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后生成的盐只有Fe(NO3)2 | B. | 反应后生成的盐只有Fe(NO3)3 | ||
| C. | 反应后生成的盐为Fe(NO3)2和Fe(NO3)3 | D. | 以上三种情况都有可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
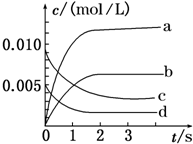 在2L密闭容器内,800℃时X(g)和Y(g)反应生成Z(g)的体系中,n(X)随时间的变化如表所示:(已知:2X(g)+Y(g)?2Z(g) )
在2L密闭容器内,800℃时X(g)和Y(g)反应生成Z(g)的体系中,n(X)随时间的变化如表所示:(已知:2X(g)+Y(g)?2Z(g) )| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(X)/mol | 0.020 | 0.010 | 0.008 | 0.008 | 0.008 | 0.008 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素符号:Cs 中文名称:铯 英文名称:Cesium 原子序数:55 相对原子质量:132.9 核外电子排布:2,8,18,18,8,1 |
| A. | 两者互为同位素 | |
| B. | 两者原子核内中子数相差3 | |
| C. | 两者氯化物的化学式都可以表示为CsCl2 | |
| D. | Cs元素位于周期表第六周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com