
【题目】一定条件下,可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是 ( )
A. 对于C2H4(g)+H2O(g)=C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1mol,则用分压表示的平衡常数Kp=![]()
B. 恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)=2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。若此时A、B和C均增加1mol,平衡正向移动
C. 一恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)=2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3molN2,则平衡正向移动
D. 对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
【答案】C
【解析】试题分析:A.平衡时C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则三者的分压均为1/3p,故用分压表示的平衡常数Kp =1/3p÷(1/3p×1/3p)=3/P,故A正确;B.如A、B和C的物质的量之比按照2:1:2的比值增加,则平衡不移动,而“均增加1mol”时相当于在原来的基础上多加了B,则平衡向右移动,故B正确;C.N2(g)+3H2(g)=2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,三者的分压均为1/3p,此时用分压表示的平衡常数为Kp=(1/3p)2/[(1/3p) ×(1/3p)3]=9/p2,若再充入3molN2,此时N2的分压为2/3p,NH3和H2均为1/6p,此时用分压表示的Qp =(1/6p)2/[(2/3p) ×(1/6p)3]=9/p2=Kp,平衡不移动,故C错误;D.同一可逆反应,在相同条件下用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,且都只与温度有关,故D正确,答案为C。


科目:高中化学 来源: 题型:
【题目】研究发现,空气之中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2=SO3+NO ②SO3+H2O=H2SO4 ③2NO+O2=2NO2 NO2在上述过程中的作用,与H2SO4在下列变化中的作用相似的是
A. 潮湿的氯气通过盛有浓H2SO4的洗气瓶 B. 硫化氢通入浓H2SO4中
C. 浓H2SO4滴入萤石中,加热 D. 加入少量H2SO4使乙酸乙酯水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,已知下列各反应为放热反应,下列各热化学方程式中ΔH最小的是
A. 2A(l)+B(l)==="2C(g)" ΔH1 B. 2A(g)+B(g)==="2C(l)"ΔH2
C. 2A(g)+B(g)==="2C(g)" ΔH3 D. 2A(l)+B(l)==="2C(l)" ΔH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见无机物A、B、C、D、E、X均由短周期元素组成,且存在如下图转化关系(部分反应物、生成物和反应条件略去)。下列推断不正确的是

A. 若D为白色沉淀,且与A的摩尔质置相等,则X—定是铝盐
B. 若A是单质,B和D的反应是OH-+HCO3-=H2O+HCO32-,则E—定能还原CuO
C. 若B、X均为单质,D为CO,C能和E反应,则E为NaOH
D. 若X是Na2SO3,C是能使品红溶液褪色的气体,则A可能是氯气,且D和E不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-![]() H++B2-,关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是
H++B2-,关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是
A.NaHB属于弱电解质
B.溶液中的离子浓度c(Na+)>c(HB-)>c(H+)>c(OH-)
C.c(Na+)=c(HB-)+c(B2-)+c(H2B)
D.NaHB和NaOH溶液反应的离子方程式为:H++OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于合金的说法不正确的是( )
A. 硬铝比纯铝的硬度低 B. 合金中可以含有非金属元素
C. 青铜是一种铜锡合金 D. 储氢合金是一类能大量吸收H2成金属氢化物的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应 Fe(s) + CO2(g) ![]() FeO(s) + CO(g),△H=aKJ﹒mol-1,平衡常数为K。测得在不同温度下,K值如下:
FeO(s) + CO(g),△H=aKJ﹒mol-1,平衡常数为K。测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.4 |
(1)若500℃时进行反应①,CO2的起始浓度为2mol﹒L-1,CO的平衡浓度为__________。
(2)该反应为__________(选填“吸热”或“放热”)反应。
(3)700℃时反应达到平衡,要使该平衡向右移动,其他条件不变时,可以采取的措施有__________(填序号)。
A.缩小反应器体积 B.CO2 C.升高温度到900℃ D.使用合适的催化剂
E.增加Fe的量
(4)下列图像符合该反应的是__________(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2)。
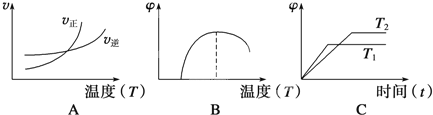
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com