
��1��д����ͼ����Ţ١������������ƣ�

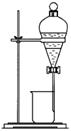
|
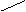
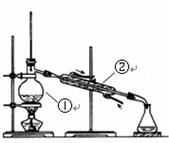
I II III
�� �� �� �� �� ��
��2�������١����У�ʹ��ʱ�������Ƿ�©ˮ���� ������������ţ�
��3����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL 1 mol�� L��1��ϡ���ᡣ
�ɹ�ѡ�õ������У��ٽ�ͷ�ι� ����ƿ ���ձ� �ܲ����� ��ҩ�� ����Ͳ ��������ƽ��
 ��ش��������⣺
��ش��������⣺
a������������ʵ���Ũ��Ϊ mol��L��1��
b������ϡ����ʱ����ȱ�ٵ������� (д��������)��
c�������㣬����480mL 1mol�� L��1��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ mL��
d���������Ƶ�ϡ������вⶨ��������Ũ��С��1 mol��L��1�����ƹ��������и�������������������ԭ���� ��������ĸ��
A������ʱ����������ƿ�̶��߽��ж���
B����ϡ�ͺ������δ����ȴֱ��ת��������ƿ��
C��ת����Һʱ��������������Һ��������ƿ����
D����������ƿ������ˮϴ�Ӻ�δ�����������������ˮ
E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��ٵ�ˮ���̶��ߴ�
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʵ�ˮ��Һ�У������ڴٽ���ˮ�ĵ���������Ե���
A��H2SO4 B��NH4Cl C��NaCl D��CH3COONa
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴Ӧ��2HI(g)  H2(g)+I2(g) ��H>0�����ܱ������н��У����ﵽƽ��ʱ��ʹ����������ɫ���Ӧ��ȡ�Ĵ�ʩ ( )
H2(g)+I2(g) ��H>0�����ܱ������н��У����ﵽƽ��ʱ��ʹ����������ɫ���Ӧ��ȡ�Ĵ�ʩ ( )
A����С������� B�������¶� C��������� D������H2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ɫ����Һ���ܴ����������( )
A.K+��Na+��HCO3����OH�� B.Cl����MnO4����K+��Na+
C.SO42����K+��Cl����NO3�� D.H+��NO3����CO32����Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�ij��̬������X���ȷֽ�ķ�ӦΪ��2XA����B����2C������÷�Ӧ�����ɵĻ��������ܶ���ͬ��ͬѹ��H2�ܶȵ�12������X��Ħ�������ǣ� ��
A��24g/mol B��48g/mol C��80g/mol D��96g/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����(HF)��һ�����ᡣ25��ʱ����20mLO.1mol•L-1������м���VmL0.1mol•L-1NaOH��Һ��ַ�Ӧ����֪: HF(aq)+OH-(aq)�TF-(aq)+H2O(1) ��H= - 67.7kJ•mol-1��
H+(aq)+OH-(aq)�TH2O(1) ��H�T - 57.3kJ•mol- �������⣬�����жϻ������ȷ����
A.�����ĵ�����������ȵ�
B.��V=20ʱ����Һ��:c(F-)��c(Na+)=0.1mol•L-1
C.��V��20ʱ����Һ������Ũ�ȹ�ϵ����Ϊ:c(Na+)=c(F-)
D.��V��20ʱ����Һ������Ũ�ȹ�ϵһ��Ϊ:c(Na+)��c(F-)��c(OH-)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2.0 mol SO2�����2.0 mol SO3�������ڹ̶�������ܱ������У���һ�������·�����Ӧ��2SO2(g)��O2(g) 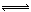 2SO3(g)���ﵽƽ��ʱSO3Ϊn mo
2SO3(g)���ﵽƽ��ʱSO3Ϊn mo l������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol����
l������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol����
A.1.6 mol SO2��0.3 mol O2��0.4 mol SO3
B.4.0 mol SO2��1.0 mol O2
C.2.0 mol SO2��1.0 mol O2��2.0 mol SO3
D.3.0 mol SO2��1.0 mol O2��1.0 mol SO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͪ(C3H6O)ͨ������ɫҺ�壬������ˮ���ܶ�С��1g��mL��1���е�ԼΪ55�档Ҫ��ˮ���ͪ�Ļ�����н���ͪ�������������Ϊ���з����������
A������ B����Һ C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ġ���ͼΪN2(g)��O2(g)��Ӧ����NO(g)�����е������仯��

����˵������ȷ����(����)
A��1 mol N2(g)��1 mol O2(g)��Ӧ�ų�������Ϊ180 kJ
B��1 mol N2(g)��1 mol O2(g)�����������2 mol NO(g)���������
C��ͨ������£�N2(g)��O2(g)�����ֱ������NO
D��NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com