
| A、用盐酸酸化的BaCl2溶液来判断亚硫酸钠固体是否发生变质 |
| B、实验室用加热NH4Cl的方法来制取氨气 |
| C、可加入足量的铜粉然后过滤来除去氯化亚铁溶液中的少量氯化铁 |
| D、加入澄清石灰水看是否有白色沉淀来区别碳酸钠溶液和碳酸氢钠溶液 |


科目:高中化学 来源: 题型:
| A、7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023 |
| B、V L a mol?L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |
| C、工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的Cu数必为0.5×6.02×1023 |
| D、标准状况下,22.4LNO和11.2L O2混合后气体的分子总数为1.0×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |

查看答案和解析>>
科目:高中化学 来源: 题型:

 +NaOH
+NaOH| CaO |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
| 实验 编号 | 铜片 质量/g | 0.1mol?L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 实验①和②探究 |
| ② | 5 | 0.5 | |||
| ③ | 5 | 20 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
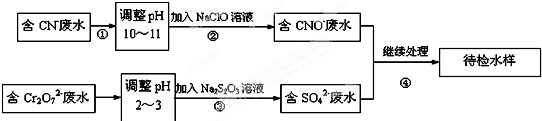
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- | ||
B、
| ||
| C、含有大量Al3+ 的溶液中:Br- HCO3- Na+ AlO2- | ||
| D、向含有Ca2+,Cl-,NO3-,Ba2+的溶液通入CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在密闭容器中通入水蒸气 |
| B、升温 |
| C、保持体积不变,充入氦气使体系压强增大 |
| D、保持压强不变,充入氦气使容器体积增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com