
已知五种短周期元素的原子序数大小顺序为C>A>B>D>E, A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出E和B形成的化合物分子含非极性共价键的结构式:____________________;
写出A、B、E形成的化合物的电子式:______________。
(2)比较A、B、C三种离子的半径大小_________________(用离子符号表示)。
(3)写出均由A、B、C、E四种元素组成的二种化合物相互反应的离子方程式
(1) H-O-O-H NaOH电子式: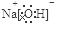 (2)S2-﹥O2-﹥Na+ (3)H++HSO3-=H2O+SO2
↑
(2)S2-﹥O2-﹥Na+ (3)H++HSO3-=H2O+SO2
↑
【解析】
试题分析:(1)短周期元素的原子序数大小顺序为C>A>B>D>E,D和E可形成4核10电子的分子。则D是N,E是H.。 A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;A是Na,B是O. B、C同主族。短周期元素中原子序数C>A>B,C是S。即A:Na,B:O.C:S,D:N,E:H.。所以E和B形成的化合物过氧化氢分子含非极性共价键的结构式:H-O-O-H。A、B、E形成的化合物NaOH的电子式: 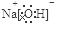
(2)S2-有3个电子层,Na+、O2-都有2个电子层,对于电子层不同的离子,离子的电子层越多,离子半径越大;对于电子层相同的离子,核电荷数越大,离子半径越小。所以这三种离子半径大小为: S2-﹥O2-﹥Na+(3)有Na、O、S 、H.四种元素组成的化合物是NaHSO4 和NaHSO3. 它们发生反应的化学方程式是NaHSO4 +NaHSO3=Na2SO4+H2O+SO2↑.离子方程式为:H++HSO3-=H2O+SO2 ↑。
考点:考查 元素周期表、元素周期律、元素推断、离子半径大小比较及离子反应等的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:






查看答案和解析>>
科目:高中化学 来源:2012-2013学年昆明三中、滇池中学(本部)高一下期中考试化学卷(带解析) 题型:单选题
已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省高三11月联考化学试卷(解析版) 题型:填空题
已知五种短周期元素的原子序数大小顺序为C>A>B>D>E, A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出E和B形成的化合物分子含非极性共价键的结构式:____________________;
写出A、B、E形成的化合物的电子式:______________。
(2)比较A、B、C三种离子的半径大小_________________(用离子符号表示)。
(3)写出均由A、B、C、E四种元素组成的二种化合物相互反应的离子方程式
查看答案和解析>>
科目:高中化学 来源:2015届福建霞浦一中高一下学期第一次月考化学试卷(解析版) 题型:选择题
已知五种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.L与T形成的化合物化学式为L2T3
B.L、M的单质与稀盐酸的反应速率:M > L
C.T、Q的氢化物常温常压下均为无色气体
D.M的最高价氧化物具有两性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com