
【题目】某有机物的结构简式如图所示,有关该有机物的叙述不正确的是
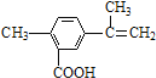
A. 在一定条件下,能发生取代、酯化和加聚反应
B. 该物质能使酸性KMnO4溶液褪色
C. lmol该物质最多可与5molH2发生加成反应
D. lmol该物质完全燃烧最多可消耗13mol氧气
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生反应2HI(g)+Cl2(g)![]() 2HCl(g) + I2(s)。下列事实不能说明该反应到平衡状态的是( )
2HCl(g) + I2(s)。下列事实不能说明该反应到平衡状态的是( )
A. 断裂1 mol Cl-Cl键同时形成1 mol H-Cl键 B. 容器内气体密度不再改变
C. 容器内气体压强不再改变 D. 容器内气体颜色不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作或现象能达到预期实验目的的是
选项 | 操作或现象 | 实验目的 |
A | 将铁钉放入试管中,用盐酸浸没 | 验证铁的吸氧腐蚀 |
B | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | 证明Br—还原性强于Cl— |
C | 将氯化亚铁固体溶于适量蒸馏水中 | 配制FeCl2溶液 |
D | 将混有氯化氢杂质的氯气通过装有饱和NaHCO3溶液的洗气瓶 | 除去氯气中的HCl气体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于过滤和蒸发说法中不正确的是( )
A. 过滤常用来分离液体与固体混合物
B. 若使溶液中的溶质析出只能选用加热蒸发的方法
C. 过滤实验用到的仪器有烧杯、漏斗、玻璃棒、铁架台等
D. 蒸发实验用到的仪器有酒精灯、蒸发皿、玻璃棒、铁架台等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 标准状况下,22.4L CCl4中含有的共价键数为4NA
B. 0.2mol NO和0.lmol O2充分反应后,混合物的分子数为0.2NA
C. 64g铜丝加热下在硫磺蒸气里完全反应后,失去的电子数为NA
D. 1 mol·L-1 Ca(ClO)2溶液中含ClO-的数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下V L氨气溶解在1L水中(水的密度近似为1g·mL-1),所得溶液的物质的量浓度为c mol·L-1,密度为ρg·mL-1,质量分数为ω,则下列关系中不正确的是( )
A. ρ=![]() B. ω=17c/1000ρ
B. ω=17c/1000ρ
C. ω=17V/(17V +22400) D. C =1000Vρ/(17V + 22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X、Y、Z为甲苯的同分异构体,Z的空间结构类似于篮子。下列说法正确的是( )
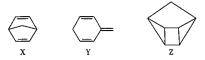
A. Z的一氯代物只有3种B. 甲苯的同分异构体只有X、Y、Z
C. X分子中所有碳原子一定在同一平面D. 1molY发生加成反应最多消耗4molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝是重要的金属材料,铁、铝及其化合物有非常重要的用途。
(1)下列说法正确的是________(填序号)。
① 配制氯化铁溶液,先将FeCl3固体溶于较浓盐酸,再用蒸馏水稀释到所需的浓度
② FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③ 利用氯水和KSCN溶液可以检验Fe3+中有无Fe2+
④ 加热蒸干Fe2(SO4)3溶液获得Fe2(SO4)3固体
⑤ 含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成Al(OH) 3的质量相等
⑥ 由于金属铝性质稳定,所以Al在空气中能稳定存在
(2)高铁酸钾(K2FeO4)是一种高效多功能水处理剂。其作用原理为__________________。
(3)以铝土矿(主要成分为Al2O3和Fe2O3、SiO2)为原料制备铝的一种工艺流程如下:
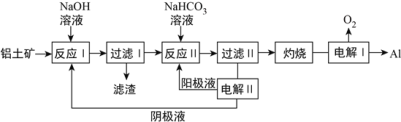
①滤渣主要成分为___________________
②在实验室灼烧操作应选择的实验仪器为_____________________
③反应II中,加入NaHCO3一段时间才有沉淀生成,写出加入少量NaHCO3时发生反应的离子方程式________。
(4)已知25 ℃时Ksp[Cu(OH)2]=2.2×1020,Ksp[Fe(OH)3]=4.0×1038, Ksp[Al(OH)3]=1.1×1033。
①在25 ℃下,向浓度均为0.1 mol·L1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式)。
②溶液中某离子物质的量浓度低于1.0×105 mol·L1时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2 mol·L1。此时所得沉淀中________(填“还含有”或“不含有”)Al(OH)3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com