
һ�ֺ��ᾧˮ����ɫ����ɱ�ʾΪA��nH2O�����нᾧˮ����������Ϊ28.57%���þ������ˮ��A��̼���⡢������Ԫ�ص����������ֱ�Ϊ26.67%��2.23%��71.1%��
�Իش��������⣺
��1������ˮ��A�����ʽ��
��2��A��NaOH��Һ�����кͷ�Ӧ��������ʽ�κ�һ�����Ρ�0.9g��ˮ��Aǡ�ú�0.1 mol��L��1NaOH��Һ200 ml ��ȫ��Ӧ�������Σ���û�����A�ķ���ʽ����ṹ��ʽ������ʾ����COOH��һ�����Թ����ţ�����д��������A������NaOH��Ӧ�Ļ�ѧ����ʽ��
��3����A��nH2O��n��ֵ��
 ��ڽ��ȫ������ϵ�д�
��ڽ��ȫ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ת���ڸ�����������ʵ�ֵ���
��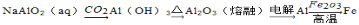
��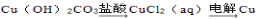
��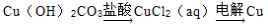
��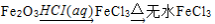
��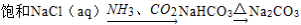
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�ƺ������ƣ�Ҳ���γɹ������������������ȷ����
A���������ƵĻ�ѧʽ��Ca2O2
B��1mol�������ƻ�������Ƹ�����ˮ��Ӧ������0.5mol����
C����������������������֮��Ϊ2��1
D������������ֻ�����Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��Ԥ�ԣ�ȼ�ϵ�ؽ��� 21 ���ͻ�õ��ܵ���Ҫ;���������꿪���ļ״�ȼ�ϵ���Dz��ò����缫����������ԭ���ǽ��缫����KOH��Һ�У�Ȼ���������ֱ����Ӽ״�����������a�������Ӽ״��� b����2H2O��O2��4e����4OH���� ���ڴ�ȼ�ϵ�ص�����˵���д������( )
A��a��������b��������
B���ŵ�����У�a��b�缫�Ͼ�����������ԭ��Ӧ��
C���õ�ع���ʱ���Ӽ״���һ����������Һ�� pH ���ͣ���Ӧ�����ӷ���ʽΪ��CH3OH��8OH���D6e����CO32����6H2O
D�����ô˵�Դ��ⱥ��ʳ��ˮ��ÿ����0.1molO2����������������0.2molCl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ��ѡ����
A������һ�������µ�ijһ���淴Ӧ����ƽ��Ũ�ȱ�ʾ��ƽ�ⳣ������ƽ���ѹ��ʾ��ƽ�ⳣ��������ֵ��ͬ����������ͬ�������¶ȵ����߶�����
B���ṹʽΪ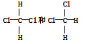 �����ʻ�Ϊͬ���칹��
�����ʻ�Ϊͬ���칹��
C�����ݷ�Ӧ��NaA+CO2(����)+ H2O==HA+NaHCO3 ; 2NaB+CO2+H2O== 2HB+Na2CO3�����Եó����ǿ����˳��Ϊ��H2CO3 �� HA�� HCO3 �� �� HB
D���������ƾ���(NaBO3��4H2O)��һ��������Ư������70�����ϼ��ȸþ���30.80�ˣ���Ӧ�������������Ϊ27.20�ˣ���ù������ʵĻ�ѧʽΪNaBO3.H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��ͼ�г��˼������ʣ��뽫���ʵĺ��������д�ڿո��ϣ�����ͬλ�ص��� ������ͬϵ����� ������ͬ���칹����� ��
�ٽ��ʯ�롰����ϩ��C 60��
��D��T��
��16O��17O����18O
��������O2���ͳ�����O3��
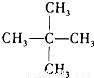
��CH4��CH3CH2CH3
���Ҵ���CH3CH2OH���ͼ��ѣ�CH3OCH3��
��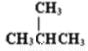 ��
��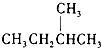
�� ��
��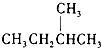
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���и����л���ֻ��һ���Լ����������
A. �Ҵ����ױ��������� B. ���Ȼ�̼�����顢��ϩ
C. �����ױ��������� D. �����Ҵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ۡ��ߺ����ö���ȼ��֮һΪLiH����֪���з�Ӧ��
��2Li(s)��H2(g)===2LiH(s)��H1����182 kJ��mol��1��
��2H2(g)��O2(g)===2H2O(l)��H2����572 kJ��mol��1��
��4Li(s)��O2(g)===2Li2O(s)��H3����1 196 kJ��mol��1��
��LiH��O2��ȼ�յ��Ȼ�ѧ����ʽΪ
A��2LiH(s)��O2(g)===Li2O(s)��H2O(l)��H����702 kJ��mol��1
B��2LiH(s)��O2(g)===Li2O(s)��H2O(l)��H����1 950 kJ��mol��1
C��2LiH(s)��O2(g)===Li2O(s)��H2O(l)��H����1 586 kJ��mol��1
D��2LiH(s)��O2(g)===Li2O(s)��H2O(g)��H����988 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������£���2 L�ܱ������г���3 mol X(g)��1 mol Y(g)���з�Ӧ��2X(g)��Y(g)  3Z(g)��2W(g)��ijʱ�̲ⶨ�����Ũ�ȣ������ܵ��ǣ� ��
3Z(g)��2W(g)��ijʱ�̲ⶨ�����Ũ�ȣ������ܵ��ǣ� ��
A��Z��0��75 mol / L B��Z��1 mol / L  C ��W��1 mol / L D��W��0��8 mol / L
C ��W��1 mol / L D��W��0��8 mol / L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com