
B环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)★ | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)★ | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7 溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应
增多。实验中将酸性Na2Cr2O7 溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7 溶液的加料方式为 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水MgSO4 固体,除去有机物中的少量水。
①上述操作的正确顺序是 (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 。
③在上述操作c中,加入NaCl 固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学
环境的氢原子。
(1)①缓慢滴加 ②环己酮和水形成具有固定组成的混合物一起被蒸出
(2)①c d b a ②漏斗、分液漏斗 ③增加水层的密度,有利于分层
(3)3
(1)①由于酸性Na2Cr2O7 溶液氧化环己醇反应剧烈,导致体系温度迅速上升、副
反应增多,所以酸性Na2Cr2O7溶液加入不能太快,应用酸式滴定管缓慢滴加。
②环己酮和水能形成具有固定组成的混合物,具有固定的沸点,蒸馏时能被
一起蒸出,所以蒸馏难以分离环己酮和水的混合物。
(2)①见答案 ②根据操作过程找出还需要的玻璃仪器有漏斗、分液漏斗。
③联系制取肥皂的盐析原理,即增加水层的密度,有利于分层。
(3)因为环己酮的结构简式为![]() ,所以环己酮分子中有3种不同化学环境的氢原子。
,所以环己酮分子中有3种不同化学环境的氢原子。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
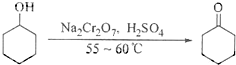
| 物质 | 沸点(℃) | 密度(g-cm-3,200C) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)* | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
A.生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式_________________________。
(2)根据等电子原理,写出CO分子的结构式______________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是_____________________;甲醛分子中碳原子轨道的杂化类型为_____________________。
②甲醛分子的空间构型是_____________________;1 mol甲醛分子中σ键的数目为_____________________。

③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为_____________________。
B.环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:

环己醇、环己酮和水的部分物理性质见下表:
物质 | 沸点(℃) | 密度(g·cm-3, | 溶解性 |
环己醇 | 161.1(97.8)* | 0.962 4 | 能溶于水 |
环己酮 | 155.6(95)* | 0.947 8 | 微溶于水 |
水 | 100.0 | 0.998 2 |
|
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的ΔH<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55~
①酸性Na2Cr2O7溶液的加料方式为_____________________。
②蒸馏不能分离环己酮和水的原因是_____________________。
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~
①上述操作的正确顺序是_______________________(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需_______________。
③在上述操作c中,加入NaCl固体的作用是_______________________________________
______________________________________________________________________________。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有______________种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省、海门中学、天一中学高三上学期联考化学试卷 题型:实验题
环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
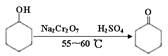
环己醇、环己酮和水的部分物理性质见下表:
|
物质 |
沸点(℃) |
密度(g·cm-3,20 ℃) |
溶解性 |
|
环己醇 |
161.1(97.8) |
0.9624 |
能溶于水 |
|
环己酮 |
155.6(95) |
0.9478 |
微溶于水 |
|
水 |
100.0 |
0.9982 |
|
括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的ΔH<0,反应剧烈将导致体系温度迅速上升,副反应增多。
实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55~60 ℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100 ℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏,收集151~156 ℃馏分
b.过滤
c.在收集到的馏分中加NaCl固体至饱和,静置,分液
d.加入无水MgSO4固体,除去有机物中少量水
①上述操作的正确顺序是 。(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 。
③在上述操作c中,加入NaCl固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源:2013届广东省高二上学期期中考试化学试卷 题型:实验题
(12分) 环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
环己醇、环己酮和水的部分物理性质见下表:
|
物质 |
沸点(℃) |
密度(g-cm-3,20℃) |
溶解性 |
|
环己醇 |
161.1(97.8)* |
0.9624 |
能溶于水 |
|
环己酮 |
155.6(95)* |
0.9478 |
微溶于水 |
|
水 |
100.0 |
0.9982 |
|
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
 (1)酸性Na2Cr2O7溶液氧化环己醇为放热反应,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物。
(1)酸性Na2Cr2O7溶液氧化环己醇为放热反应,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为 。
 ②蒸馏不能分离环己酮和水的原因是 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a蒸馏,收集151-156℃的馏分;
b 过滤;
c 在收集到的馏分中加NaCl固体至饱和,静置,分液;
d 加入无水MgSO4固体,除去有机物中少量水。
 ①上述操作的正确顺序是
(填字母)。
①上述操作的正确顺序是
(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 、 。
 ③在上述操作c中,加入NaCl固体的作用是
。
③在上述操作c中,加入NaCl固体的作用是
。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学环境的氢原子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com