(2009?广东)超细氧化铝是一种重要的功能陶瓷原料.
(1)实验室常以NH
4Al(SO
4)
2和NH
4HCO
3为原料,在一定条件下先反应生成沉淀NH
4AlO(OH)HCO
3该沉淀高温分解即得超细Al
2O
3.NH
4AlO(OH)HCO
3热分解的化学反应方程式
2NH
4AlO(OH)HCO
3
Al
2O
3+3H
2O↑+2CO
2↑+2NH
3↑
2NH
4AlO(OH)HCO
3
Al
2O
3+3H
2O↑+2CO
2↑+2NH
3↑
.
(2)NH
4Al(SO
4)
2?12H
2O的相对分子质量为453.欲配制100mLPH为2、浓度约为0.1mol
-1的NH
4Al(SO
4)
2溶液,配制过程为
①用托盘天平称量NH
4Al(SO
4)
2?12H
2O固体
4.5
4.5
g;
②将上述固体置于烧杯中
用量筒量取100mL水,搅拌溶解,用H2SO4调节溶液PH至2
用量筒量取100mL水,搅拌溶解,用H2SO4调节溶液PH至2
.
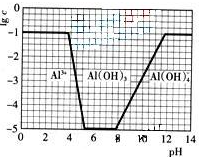
(3)在0.1mol?L
-1NH
4Al(SO
4)
2溶液中,铝各形态的浓度(以Al
3+计)的对数(lgc)随溶液PH变化的关系见下图
①用NaOH溶液调节(2)中溶液PH至7,该过程中发生反应的离子方程式有
H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3?H2O
H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3?H2O
.
②请在答题卡的框图中,画出0.01mol?L
-1NH
4Al(SO
4)
2溶液中铝各形态的浓度的对数lgc随溶液PH变化的关系图,并进行必要的标注.

 (2009?广东)超细氧化铝是一种重要的功能陶瓷原料.
(2009?广东)超细氧化铝是一种重要的功能陶瓷原料. Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑ Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑ Al2O3+3H2O+2CO2↑+2NH3↑,故答案为:2NH4AlO(OH)HCO3
Al2O3+3H2O+2CO2↑+2NH3↑,故答案为:2NH4AlO(OH)HCO3 Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑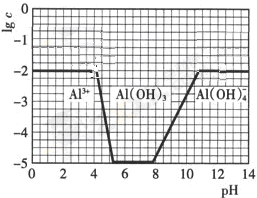 ,故答案为:
,故答案为:

