
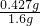 ×100%=26.7%,
×100%=26.7%,

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:填空题
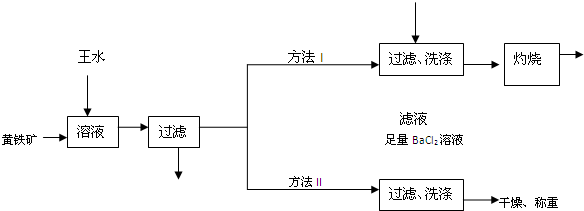
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:

查资料得知:
|
物质名称 |
溶度积(Ksp) |
pH值 |
|
|
开始沉淀 |
完全沉淀 |
||
|
Mg(OH)2 |
5.6×10-12 |
9.3 |
10.8 |
|
Fe(OH)3 |
2.8×10-16 |
2.7 |
3.7 |
|
Al(OH)3 |
1.3×10-33 |
3.7 |
4.7 |
请回答下列问题:
(1)写出固体A的化学式为 。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是 。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E ; ②溶液F生成固体G 。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为 。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)“化学――人类进步的关键”。日常生活、社会生产中的许多问题都涉及到化学知识。下列有关说法中正确的是(填序号,多选倒扣分)___________________________________________。
A、冰的密度小于液态水,氨易液化,均与氢键有关
B、明矾净水,血液透析,均与胶体知识有关
C、从经济效益等方面综合考虑,硫酸厂在常压和合适温度下催化氧化SO2,且应在距离原料产地近的地方建厂
D、我国生产硫酸的主要原料是黄铁矿、水、空气
E、生产水泥、玻璃的共同原料是石灰石
F、用除去油污的废铁屑与过量的稀硫酸制备绿矾(FeSO4?7H2O)
G、晶体硅常用作光导纤维材料
H、氯碱工业中用阳离子交换膜将电解槽分为阳极室和阴极室,精制饱和食盐水送入阴极室
I、干冰、溴化银常用于人工降雨
J、硫酸铜晶体中结晶水含量测定实验中至少加热2次,称量4次
(Ⅱ)、某无色混合气体可能含有CO2、CO、H2O(气)、H2中的一种或几种,依次进行如下处理(假定每步处理均反应完全)。(1)通过碱石灰时,气体体积变小;(2)通过赤热的CuO时,固体变为红色;(3)通过白色CuSO4粉末时,粉末变为蓝色;(4)通过澄清的石灰水时,溶液变浑浊。由此可以确定原混合气体的成分可能是(已给出一种可能,还有几种可能就填几种,可不填满)。CO、H2、CO2、、______________、_______________、_______________、_____________、_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com