
(16分)根据铜锌原电池示意图,回答下列问题: 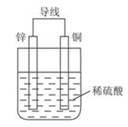
(1)锌为 极,电极反应式为 ;铜为 极,电极反应为 ,原电池总离子反应式是 。
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量 (填“增加”、“不变”或“减少”);电子从电池的锌极沿导线流向电解池的 (填“阴极”或“阳极”,下同);在电解池中Cu2+向 移动,在该电极上析出铜的质量为 g。
科目:高中化学 来源: 题型:阅读理解
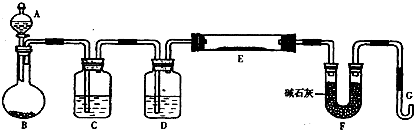
| 24(c-a) |
| b-c |
| 24(c-a) |
| b-c |
| 27(c-a) |
| e-d |
| 27(c-a) |
| e-d |
| 27(b-a) |
| e-d |
| 27(b-a) |
| e-d |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:2014届广东省高一6月月考理科综合化学试卷(解析版) 题型:填空题
(16分)根据铜锌原电池示意图,回答下列问题:
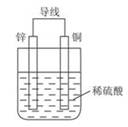
(1)锌为 极,电极反应式为 ;铜为 极,电极反应为 ,原电池总离子反应式是 。
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量 (填“增加”、“不变”或“减少”);电子从电池的锌极沿导线流向电解池的 (填“阴极”或“阳极”,下同);在电解池中Cu2+向 移动,在该电极上析出铜的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com