
【题目】下列实际问题,不涉及到盐类水解原理的是( )
A. 草木灰不宜与铵态氮肥混合施用B. 用醋酸清洗保温瓶里的水垢
C. 配制FeCl3溶液时加入适量的盐酸D. 用热的纯碱溶液洗涤油污效果较好
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空
(1)书写下列物质电子式
①Cl2:_______________; ②CO2:_______________; ③NaOH:_______________;
④Na2S:_______________; ⑤H2O2:_______________;
(2)用电子式表示下列物质的形成过程
①MgCl2:___________________________________________________;
②H2O:_____________________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钻及其化合物属于2B类致癌物,但它们广泛应用于实验室研究及工业生产的磁性材料领域。
(1)干燥剂变色硅胶常含有CoCl2固体。常见氯化钻晶体的颜色如下:

则硅胶吸水饱和之后颜色变成_____________。
(2)CoxNi(Ⅱ)(1-x)Fe(Ⅲ)2O4中Co的化合价为________。(Ⅱ、Ⅲ表示Ni、Fe元素的化合价)
(3)CoxNi(1-x)Fe2O4对催化分解H2O2具有较高的活性。单位质量的CoxNi(1-x)Fe2O4在10℃时催化分解6%H2O2溶液的初始速率随x变化的曲线如图(其中实线使用的催化剂是微波水热法合成的,虚线使用的催化剂是常规水热法合成的)。由图中信息可知影响催化剂活性大小的因素有催化剂的合成方法和__________________________。

(4)草酸钴是制备钴的氧化物的重要原料,其热分解过程除受草酸钴本身性质的影响之外,还受反应气氛和反应温度的影响。二水合草酸钴(CoC2O42H2O)在空气中热分解的分析曲线如图所示,已知Co的两种常见化合价为+2价和+3价,曲线中300℃以上所得固体为钴的氧化物

①A点剩余固体的主要成分为__________________________。
②225~300℃发生反应的化学方程式为_____________________________。
③C点钻的氧化物可与浓盐酸反应生成黄绿色气体,写出该反应的离子方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一包固体粉末,可能含有![]() 、KOH、
、KOH、![]() 、
、![]() 、
、![]() 中的一种或几种。某同学为探究固体粉末的组成,取适量样品进行如下实验。
中的一种或几种。某同学为探究固体粉末的组成,取适量样品进行如下实验。

下列说法不正确的是![]()
![]()
A. 固体粉末中一定不含KOH
B. 固体粉末中一定含有![]() 和
和![]()
C. 取溶液1先加足量盐酸酸化,再加氯化钡溶液,若未产生白色沉淀,则样品中无硫酸钠
D. 为进一步确定原样品组成,可以向固体2中加入NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍,A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73.2%和7.32%。
(1)A的分子式是__;
(2)已知:
ⅰ.![]() (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
ⅱ.![]()
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是__;
②若G为气体,且相对分子质量是44,则E的结构简式是__;E的核磁共振氢谱中有__个吸收峰(填数字);
③F→H的反应类型是__;
④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式__;
⑤A的结构简式是__;
上述转化中B→D的化学方程式是__;
(3)已知A的某种同分异构体K具有如下性质:
①K与FeCl3反应,溶液呈紫色
②K在一定条件下可发生银镜反应
③K分子中苯环上的取代基上无甲基
请写出K所有可能的结构简式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语中,正确的是( )
A. 次氯酸的结构式:H—O—Cl
B. 氮气的电子式:∶N∶∶∶N∶
C. CO2分子的电子式:O=C=O
D. 用电子式表示氯化氢分子的形成过程:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列流程图。
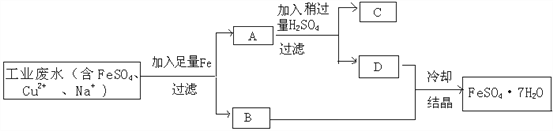
(1)其中,滤渣A中有______________,滤液D中溶质有________________。(填化学式)
(2))加入Fe的目的是_______________________________________。(用化学方程式表示)
(3)加入H2SO4的目的是____________________________________。(用化学方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通信是一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的( )
A.碳B.石英C.锗D.硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在工业生产中具有十分重要的意义。
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___________________________。
(2)已知反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
FeO(s)+CO(g) ΔH=a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
温度(℃) | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
①该反应的化学平衡常数K的表达式为____________,a________0(填“>”、“<”或“=”)。在500 ℃ 2 L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5 min后达到平衡时CO2的转化率为________,生成CO的平均速率v(CO)为_______________。
②700 ℃反应达到平衡后,要使反应速率增大且平衡向右移动, 可采取的措施有 ___________。
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式_____________________,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=_________(溶液电解前后体积的变化忽略不计)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com