
Z��Y��X��W��V��ԭ������������������ֳ���Ԫ�ء�XԪ���ǵؿ��к�������Ԫ�أ�Y��Z��ɵ���̬������M��ˮ��Һ�ʼ��ԣ�W�ĵ�����X2��ȼ�ղ����ʹƷ����Һ��ɫ��V��һ����ʷ�ƾá�Ӧ�ù㷺�Ľ���Ԫ�ء���ش�
��1��YԪ�������ڱ��е�λ���� ��M�ķ��ӿռ乹��Ϊ �Σ�M�� ���ӣ������ԡ��Ǽ��ԡ���
��2��д��X��Z����Ԫ����ɵĻ�����Z2X2�Ľṹʽ�� ��
��3������������Ԫ������������γɵĻ������У���һ����������ˮ��Ӧ���������ҷ�Ӧ����������ԭ��Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ ��
��4��X��Y��Z����Ԫ�ؿ����һ��ǿ��U��M��U��Ӧ����һ����K,д��K�к��еĻ�ѧ������ ��
��5������V����Ͷ�뵽������Һ�У�������dz��ɫ��ҺN��N��������Һ��˫��ˮ��Ӧ�����ӷ���ʽ�� ��
��1���ڶ����ڣ�VA�壨1�֣���һ������0�֣� ������1�֣� �Ǽ��ԣ�1�֣�
��2��H-O-O-H��1�֣�
��3��3NO2+H2O=2HNO3+NO��2�֣�
��4�����Ӽ� ���ۼ� ��λ������λ����д���۷֣� ��2�֣�
��5��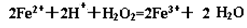 ��2�֣� ��2�֣�
��2�֣� ��2�֣�
��������
���������XΪ����YΪ����ZΪ�⡢MΪ������WΪ�ơ�VΪ������1������ϵ�����ڵ��Ӳ����������������������������ʵ���Ԫ�����ڱ��е�λ��Ϊ�ڶ����ڣ�VA��,����Ϊ�����εĶԳƽṹ�����ڷǼ��Է��ӡ���2��˫��ˮ���ڹ��ۻ������ṹΪH-O-O-H����3����Ԫ�ػ��ϼ������뽵�͵ķ�Ӧ������������ԭ��Ӧ���ʸ÷�ӦΪ3NO2+H2O=2HNO3+NO����4�������⡢����ɵ���Ϊ���ᣬ�����백����Ӧ��������泥���KΪ����泥�������д������Ӽ� ���ۼ� ��λ������5���������ᷴӦ�����Ȼ��������������������Ӿ��л�ԭ�ԣ�˫��ˮ���������ԣ���˿���������������Ϊ+3�۵������ӣ������ӷ�Ӧ����ʽΪ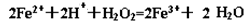
���㣺��Ҫ���������ƶϵ����֪ʶ�㣬�Ѷ����У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������������ȷ����
A����100ml��Ͳ��ȡ8.5ml��ˮ
B��Ϊ�˲�����˷ѣ�ʵ��ʣ���ҩƷ�Ż�ԭƿ
C�����ձ����ڵ���ʯ��������Ȧ�ϼ���
D����ȼ�ŵľƾ���ȥ��ȼ��һ�ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���ຣʡ�����и�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A������ȼ��ʱ��ȫ���Ļ�ѧ��ת��Ϊ����
B����AgCl��Һ�м������ᣬKsp���
C�������ڼ�������R2-����Rһ������VIA��
D�������������ٵĽ���Ԫ�أ�һ����������������Ľ���Ԫ�ػ�����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ�������ɽ�ظ�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У��������뻹ԭ�����ʵ����Ĺ�ϵΪ1��2����
A��4HCl+MnO2===MnCl2+Cl2��+2H2O
B��I2+2NaClO3===2NaIO3+Cl2
C��2CH3COOH+Ca(ClO)2===2HClO+Ca(CH3COO)2
D��Fe + 2H+===2Fe2+ + H2 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ�������ɽ�ظ�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У�����ȷ����
A��������Ư�۾�����������ˮ��ɱ��������
B�����ά����Ҫ�ɷ���SiO2
C���������մɶ����ڴ�ͳ�����β���
D�������ŷ�SO2����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���20��00 mL 1��000 mol��L��1��ˮ�е���1��000 mol��L��1���ᣬ��ҺpH���¶��������������仯������ͼ��ʾ�������й�˵���������

A��a��d�������Һ��ˮ�����ӻ�Kw(a)>Kw(d)
B�����˰�ˮϡ�ͣ���Һ�ĵ�����������
C��c��ʱ�����������V(HCl)<20 mL
D�������£�a��İ�ˮ���볣��Ϊ mol��L��1
mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ȷ����
A��AlCl3��Һ�м��������ˮ��Al3����4NH3��H2O=== ��2H2O��
��2H2O��
B�����Ƶ�ˮ�ⷴӦ��S2����2H2O H2S��2OH��
H2S��2OH��
C��������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba(OH)2��Һ��� ��Ba2����OH��===BaCO3����H2O
��Ba2����OH��===BaCO3����H2O
D������ͭ��ϡ���ᷴӦ��Cu��2H���� ===Cu2����2NO����H2O
===Cu2����2NO����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
������25 ��ʱ�������ܵ���ʵ��ܽ�ȣ�
���ܵ���� | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
�ܽ��/g | 9��10-4 | 1��7��10-6 | 1��5��10-4 | 3��0��10-9 |
������������ᴿ�У����������ܵ���ʵ��ܽ�ƽ��ԭ����ȥijЩ�������ӡ����磺
��Ϊ�˳�ȥ�Ȼ���е�����Fe3+���Ƚ����������ˮ���ټ���һ�������Լ���Ӧ�����˽ᾧ���ɣ�
��Ϊ�˳�ȥ�Ȼ�þ�����е�����Fe3+���Ƚ����������ˮ������������������þ����ַ�Ӧ�����˽ᾧ���ɣ�
��Ϊ�˳�ȥ����ͭ�����е�����Fe2+���Ƚ����������ˮ������һ������H2O2����Fe2+������Fe3+��������Һ��pH=a�����˽ᾧ���ɡ�
��ش��������⣺
��1���������ֳ��ӷ������ܹ��ﵽ�ܺõ�Ч����Fe3+��Fe2+����ת��Ϊ (�ѧʽ)����ȥ��
��2�����м�����Լ�Ӧ��ѡ�� Ϊ�ˣ���ԭ���� ��
��3�����г�ȥFe3+���������ܷ�Ӧ�����ӷ���ʽΪ ��
��4����֪Fe(OH)3��Ksp=1��10-35mol4/L4 ����ѧ��ͨ����Ϊ��������Һ������Ũ��С��1��10-5mol/Lʱ��������ȫ����������a��СֵΪ .
��5�������뷽������ص������У���ȷ���� (����ĸ)��
A��H2O2����ɫ�������������������в��������ʣ���������Ⱦ
B����Fe2+����ΪFe3+����Ҫԭ����Fe(OH)2������Fe(OH)3�������ѹ���
C��������ҺpH=a��ѡ����Լ���������ͭ���ʽ̼��ͭ
D��Cu2+���Դ���������pH=a����Һ��
E����pH>a����Һ��Fe3+һ�����ܴ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A������Ħ�������һ����22.4 L/mol
B��1 mol H2O(g)�ڱ�״�������Ϊ22.4 L
C��1 mol�������Ϊ22.4 L����һ���DZ�״��
D��1 mol�κ�������ռ�����Լ��22.4 L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com