
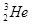 核聚变所释放出的能量相当于目前人类一年消耗的能量,在地球上氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量,在地球上氦元素主要以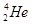 的形式存在。有关该元素说法正确的是
的形式存在。有关该元素说法正确的是A.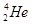 原子核内有4个质子 原子核内有4个质子 |
B.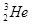 和 和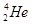 互为同位素 互为同位素 |
C.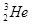 原子核内有3个中子 原子核内有3个中子 |
D.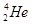 最外层只有2个电子故具有较强的金属性 最外层只有2个电子故具有较强的金属性 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
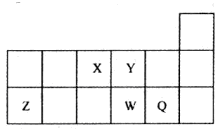
| A.元素W的最高价氧化物对应的水化物的酸性比Q的强 |
| B.原子半径的大小顺序为:X>Y>Z>W>Q |
| C.离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| D.元素Y与元素W的最高化合价的数值等于其族序数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
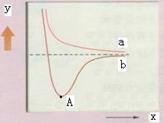
| A.y代表两原子之间的核间距 |
| B.x代表体系具有的能量 |
| C.a代表核外电子自旋相反的两个氢原子能量变化 |
| D.A点时表示两原子间形成了稳定的共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是空气中含量最丰富的元素 |
| C | 短周期中,单质C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与镓同主族且相邻周期的元素,其原子序数为23或49 |
| B.与镓同周期且相邻主族的元素,其原子序数为30或32 |
| C.原子半径:Br>Ga> Cl> Al |
| D.碱性:KOH>Ga(OH)3>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸A中X的化合价比酸B中Y化合价高 |
| B.酸A中X与酸B中Y在同一周期,且X在Y之后 |
| C.酸A与酸B的铵盐溶液反应生成酸B |
| D.酸A具有强氧化性,酸B没有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子结构随着元素原子序数的递增而呈周期性变化,这个规律叫元素周期律 |
| B.第三周期元素的简单离子半径随原手序数的递增依次增大 |
| C.第ⅦA族元素的简单阴离子还原性越强,其气态氢化物的稳定性越弱 |
| D.16O2与18O2互为同位素,它们的性质基本相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
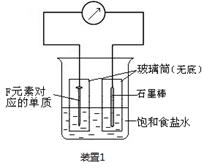
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com