
【题目】“摩尔庄园”是一款专门为7—12岁儿童(也就是说并不适合很大年齡的你们)安全健康益智网页游戏,它和我们化学高大上的摩尔没有半毛钱的关系,你们总是学不会的“摩尔”其实是指( )
A. 国际单位制中的一个物理量 B. 摩尔是表示物质的量
C. 摩尔是物质的量的单位 D. 摩尔是表示物质数量的单位
科目:高中化学 来源: 题型:
【题目】下列关于油酯的叙述中不正确的是( )
A. 油酯属于酯类 B. 油酯没有固定的熔、沸点
C. 油酯都不能使溴水褪色 D. 油酯是高级脂肪酸的甘油酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1mol HNO3的质量是____________, 1mol HNO3含有_____mol氧原子。
(2)标准状况下11.2L HCl气体溶于水中配成1L溶液,所得盐酸溶液的物质的量浓度是_______________。
(3)2mol OH 约含有__________________个电子。
(4)9.5gMgCl2固体溶于水配成500mL溶液,其中Cl-浓度为________mol· L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国对‘可呼吸”的钠-二氧化碳电池的研究取得突破性进展。该电池的总反应式为:4Na+3CO2 ![]() 2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
2Na2CO3+C,其工作原理如下图所示(放电时产生Na2CO3固体储存于碳纳米管中)。下列说法不正确的是
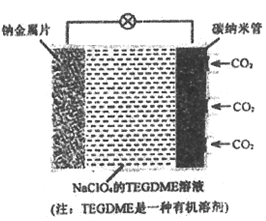
A. 放电时,钠金属片作负极,碳纳米管作正极
B. 充电时,阳极反应为:2Na2CO3+C-4e-=3CO2↑+4Na+
C. 放电时,Na+从负极区向正极区移动
D. 该电池的电解质溶液也可使用NaClO4的水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果发现了原子序数为116的元素,下列叙述不正确是
①位于第七周期;
②是非金属元素;
③最外电子层含有6个电子;
④没有放射性;
⑤属于氧族元素;
⑥属于卤素。
A. ②④⑥ B. ①③⑥ C. ①③⑤ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 聚四氟乙烯的单体属于不饱和烃
B. 苯乙烯分子的所有原子不可能在同一平面上
C. 分子式为C4H10O属于醇的同分异构体有4种
D. 异丁烯及甲苯均能使溴水褪色,且褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源。

(1)填充物用60℃温水溶解,目的是_________。
(2)铜帽溶解完全后,可采用______方法除去溶液中过量的H2O2。
(3)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。其正极的电极反应式为______________。
(4)锌锰干电池所含的汞可用KMnO4溶液吸收。在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如下图所示:

根据上图可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率_______。
②在pH为12~14条件下,KMnO4溶液吸收Hg的化学方程式________。
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀破酸、稀草酸,并不断搅拌至无气泡为止。主要反应为: 2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O。
①当1mol MnO(OH)参加反应时,共有______mol电子发生转移。
②已知:MnCO3和Mn(OH)2的Ksp分别是9×10-11、4×10-14。工业上向上述所得的MnSO4溶液中加入NH3和NH4HCO3来制备碳酸锰, 若溶液中Mn2+为1.0mol·L-1,为尽可能多的获得高纯碳酸锰,应控制溶液中c(CO32-)_______≥mol·L-1,过程中应控制pH<_______。[Mn2+沉淀完全;lg2=0.3]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钙是一种重要的化工原料,制备CaBr2·2H2O 的主要流程如下:
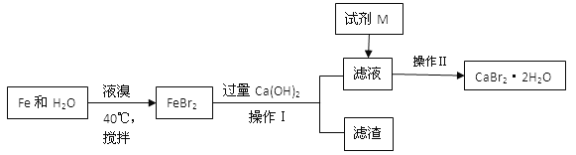
下列说法不正确的是
A. 试剂M 是HBr,加入HBr的目的是除去过量的Ca(OH)2
B. 操作I为过滤,滤渣为Fe、Fe(OH)2和Fe(OH)3;操作Ⅱ为重结晶,具体操作步骤为蒸发浓缩、冷却结晶、洗涤、干燥
C. 制得的CaBr2·2H2O 可以通过以下方法测定纯度:称取一定量的样品溶于水,滴入足量Na2CO3 溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却、称量,计算便得出CaBr2·2H2O的纯度
D. 工业上也可以将氨气通入石灰乳,并加入溴,于65℃进行反应,制得溴化钙,此反应中还会生成一种无色气体,该反应的化学方程式为3Ca(OH)2+3Br2+2NH3 ![]() 3CaBr2+N2+6H2O
3CaBr2+N2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com