
【题目】碘在科研与生活中有重要应用.某兴趣小组用0.50molL﹣1KI、0.2%淀粉溶液、0.20molL﹣1K2S2O8、0.10molL﹣1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.已知: S2O82﹣+2I﹣═2SO42﹣+I2(慢) I2+2S2O32﹣═2I﹣+S4O62﹣(快)
(1)向KI,Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的耗尽后,溶液颜色将由无色变成为蓝色.其中该反应速率快慢的是由(填“第一个”或“第二个”)反应决定的.为确保能观察到蓝色,S2O32﹣与S2O82﹣初始的物质的量需满足的关系为:n(S2O32﹣):n(S2O82﹣) .
(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积/mL溶液 | ||||
K2S2O8溶液 | H2O | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | V1 | V3 | 4.0 | 2.0 |
③ | 8.0 | V2 | V4 | V5 | 2.0 |
表中V3、V4和V5取实验设计的体积数值,目的是 , 表中的V2= , 理由是 .
【答案】
(1)S2O32﹣或Na2S2O3;第一个;<2:1
(2)探究K2S2O8浓度对反应速率的影响,KI溶液、Na2S2O3溶液用量相等;2.0;保证溶液总体积不变,即其他条件不变,只改变反应物K2S2O8浓度,从而才达到对照实验目的(3)已知某条件下,浓度c(S2O82﹣)~反应时间t的变化曲线如图13,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度(曲线a)和加入催化剂(曲线b)时c(S2O82﹣)~t的变化曲线示意图. 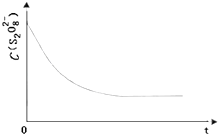
解:保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短,降低反应温度和加入催化剂时c(S2O82﹣)~反应时间t的变化曲线示意图为: 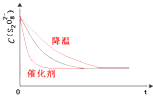
【解析】解:(1)慢反应中有I2生成,使溶液变蓝色,而快反应中消耗I2 , 慢反应决定反应速率,当溶液中的 S2O32﹣或Na2S2O3耗尽后,碘才能与淀粉作用显示蓝色; 根据I2+2S2O32﹣═S4O62﹣+2I﹣ (快)可知,1mol碘需2molS2O32﹣ , 根据方程式S2O82﹣+2I﹣═2SO42﹣+I2可知,生成1mol碘需为1molS2O82﹣ , 为确保能观察到蓝色,碘需有剩余,即n(S2O32﹣):n(S2O82﹣)<2:1,
所以答案是:S2O32﹣或Na2S2O3;第一个;<2:1;(2)实验目的是探究反应物浓度对化学反应速率的影响,由表中数据可知,KI溶液、Na2S2O3溶液用量相等,应是探究K2S2O8浓度对反应速率的影响,保持溶液总体积相等,即其他条件不变,只改变反应物K2S2O8浓度,从而才达到对照实验目的,故Vx=10.0mL﹣8.0mL=2.0mL,
所以答案是:探究K2S2O8浓度对反应速率的影响,KI溶液、Na2S2O3溶液用量相等;2.0;保证溶液总体积不变,即其他条件不变,只改变反应物K2S2O8浓度,从而才达到对照实验目的;(3)保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短,降低反应温度和加入催化剂时c(S2O82﹣)~反应时间t的变化曲线示意图为: ,
,
所以答案是:  .
.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并注明反应类型
(1)由丙烯制备聚丙烯的反应反应类型
(2)用甲苯制TNT的反应反应类型
(3)苯制溴苯反应类型
(4)乙烯通入溴水中反应类型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了如下装置制取和验证SO2的性质。

请回答:
(1)写出图中仪器的名称:a___________,b___________。
(2)棉球中NaOH溶液的作用是______________________。
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_____________________。
A.紫色石蕊试液 B.无色酚酞试液 C.澄清石灰水 D.碘水
(4)下列说法正确的是____________。
A.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
B.先向装置中加入试剂(药品),再进行气密性检查
C.实验开始后,洗气瓶①和③只溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)洗气瓶④中发生反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molCO和1molH2O充入容器中,在催化剂存在下发生反应H2O (g)+CO(g)H2 (g)+CO2(g)达到平衡时,发现有50%的CO转化为CO2 . 在其他条件不变的情况下,若将1molCO和3molH2O充入反应器中,则反应达平衡后,求:
(1)达平衡后CO的转化率
(2)混合气体中CO2体积分数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图的所示的转化关系。由此推断:

(1)甲的化学式为_____________,丙的化学式为______________。
(2)写出甲和D反应的化学方程式___________________________________________。
(3)为检验化合物甲中元素的化合价,需要用到的药品有_________________________。
A.稀硫酸 B.盐酸 C.硫氰化钾溶液 D.高锰酸钾溶液
(4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:
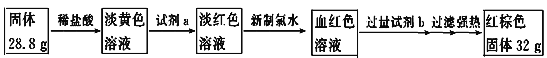
化合物甲的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按照要求完成下列方程式。
(1)工业制取氯气的离子反应方程式:________________________________________。
(2)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:______________________________________。
(3)澄清石灰水中通入CO2变浑浊又变澄清的反应方程式:__________________________________________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温条件下,将1molNO2充入一恒容密闭容器中,进行如下反应:2NO2(g)═N2O4(g)△H<0则该条件下,如下示意图中正确且能说明反应达到平衡状态的是( )
A.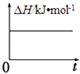
B.
C.
D.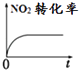
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com