
| A. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 碳酸钡溶于稀硝酸:BaCO3+2H+=Ba2++CO2↑+H2O | |
| C. | 实验室用大理石与盐酸反应制取二氧化碳:CO32-+2H+=CO2↑+H2O | |
| D. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ |
分析 A.反应生成硫酸亚铁和氢气;
B.反应生成硝酸钡、水、二氧化碳;
C.碳酸钙在离子反应中保留化学式;
D.电子不守恒.
解答 解:A.铁和稀硫酸反应的离子反应为Fe+2H+=Fe2++H2↑,故A错误;
B.碳酸钡溶于稀硝酸的离子反应为BaCO3+2H+=Ba2++CO2↑+H2O,故B正确;
C.实验室用大理石与盐酸反应制取二氧化碳的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故C错误;
D.钠与水的反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯、乙醇均能使酸性高锰酸钾溶液褪色 | |
| B. | 通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷 | |
| C. | 乙烯、环己烷都属于烃类,它们通式相同,但它们不互为同系物 | |
| D. | 烯烃完全燃烧时,生成CO2和H2O的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若增大压强,则混合气体的平均分子量减小 | |
| B. | 将容器体积变为0.5 L,Z的平衡浓度变为原来的2倍 | |
| C. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| D. | 保持体积不变,向其中充入1 mol He气体,平衡右移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
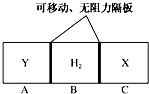 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入均为10g的X、Y两种气体,且测得二者的密度相等.当隔板停止滑动时,下列说法一定正确的是( )| A. | X、Y均为气体单质 | |
| B. | X、Y的相对分子质量相等 | |
| C. | n(H2)<n(X)=n(Y) | |
| D. | 隔板停止滑动时,A、B、C三部分体积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2→O2的变化过程中,必须要加入合适的氧化剂才能实现 | |
| B. | Al2O3+3C+N2═2AlN+3CO中,Al2O3是氧化剂 | |
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑中MnO2是还原剂 | |
| D. | 有金属单质参加的反应中,金属单质一定作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com