
| A. | 0.01mol•L-1 | B. | 0.05mol•L-1 | C. | 0.017mol•L-1 | D. | 0.50mol•L-1 |
分析 物质的量浓度相等的NaOH和HCl溶液,以3:2体积比相混合,发生反应:NaOH+HCl=NaCl+H2O,氢氧化钠有剩余,令二者的浓度为cmol/L,用c表示出反应后溶液中c(OH-),根据混合后溶液的pH=13,可知应后溶液中c(OH-)=0.1mol/L,据此计算.
解答 解:物质的量浓度相等的NaOH和HCl溶液,以3:2体积比相混合,发生反应:NaOH+HCl=NaCl+H2O,氢氧化钠有剩余,令二者的浓度为cmol/L,则反应后溶液中c(OH-)=$\frac{3c-2c}{3+2}$mol/L=$\frac{c}{5}$mol/L,根据混合后溶液的pH=13,可知应后溶液中c(OH-)=0.1mol/L,即$\frac{c}{5}$mol/L=0.1mol/L,解得c=0.5,
故选D.
点评 本题考查溶液pH值的有关计算,难度不大,注意酸碱混合后呈碱性,先计算剩余氢氧根的浓度,再计算氢离子浓度,利用定义计算pH值.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学平衡常数表达式为:K=$\frac{c(CO)•({H}_{2}O)}{c(C{O}_{2})•({H}_{2})}$ | |
| B. | 升高温度,正反应速率增大,逆反应速率减小 | |
| C. | 容器内CO和H20的浓度始终相等 | |
| D. | 容器内的压强始终不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
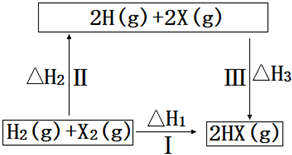
| A. | 2H(g)+2X(g)=2HX(g)△H3<0 | |
| B. | 途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 | |
| C. | 途径Ⅰ生成HBr放出的热量比生成HCl的少,说明HBr比HCl稳定 | |
| D. | Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下,0.1 mol•L-1 HA溶液的pH=3,则HA的电离:HA=H++A- | |
| B. | 用铜电极电解饱和硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 向1 mL 2 mol•L-1NaOH溶液中滴加1~2滴0.1 mol•L-1MgCl2溶液后,再滴加2滴0.1 mol•L-1 FeCl3溶液:Mg2++2OH-═Mg(OH)2↓,3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 钢铁发生吸氧腐蚀生成铁锈:2Fe+O2+2H2O═2Fe(OH)2,4Fe(OH)2+O2+2H2O═4Fe(OH)3,2Fe(OH)3═Fe2O3•xH2O+(3-x)H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的NaHSO4溶液:c(Na+)+c(H+)=2c(SO42-)+c(OH-) | |
| B. | 0.1 mol/L NaHCO3溶液加水稀释后,c(H+)与c(OH-)的乘积不变 | |
| C. | pH相同的①CH3COONa、②NaClO二种溶液的c(Na+):①<② | |
| D. | 0.1 mol/L Na2SO3溶液:c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 |
| 沉淀物 | CuS | ZnS | MnS | FeS | ||
| Ksp | 8.5×10-45 | 1.2×10-23 | 1.4×10-15 | 3.7×10-14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com