
【题目】下列说法中正确的是( )
A.按系统命名法,化合物![]() (键线式结构)的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
(键线式结构)的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
B.环己烯与化合物 (键线式结构)互为同系物
(键线式结构)互为同系物
C.分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若将所有可能得到的醇和酸重新酯化,可形成的酯共有16种
D.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等
【答案】D
【解析】
试题分析:A.根据结构简式判断有机物主链碳原子数以及支链的种类和数目,可命名;
B.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
C.分子式为C4H8O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为4,讨论羧酸与醇含有的碳原子,判断形成该酯的羧酸与醇的同分异构体种数,根据羧酸与醇组合,计算同分异构体数目;
D.根据分子式计算即可.
解:A.由结构简式可知有机物主链含有6个碳原子,含有4个甲基、2个乙基,名称为2,2,4,5﹣四甲基﹣3,3﹣二乙基己烷,故A错误;
B.环己烯中只含有一个碳碳双键,与所给的物质结构不相似,不是同系物,故B错误;
C.分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,属于饱和一元酯,若为甲酸和丙醇酯化,甲酸1种,丙醇有2种;若为乙酸和乙醇酯化,乙酸1种,乙醇有1种;若为丙酸和甲醇酯化,丙酸有1种,甲醇1种,故羧酸共有3种,醇共有4种,酸和醇重新组合可形成的酯共有3×4=12种,故C错误;
D.苯和苯甲酸的分子式分别为C6H6、C7H6O2,C7H6O2可看作C6H6CO2,由分子式可知等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故D正确,故选D.


科目:高中化学 来源: 题型:
【题目】Ⅰ.由苯乙烯制得的聚苯乙烯可用于制造一次性餐具.![]()
(1)苯乙烯的分子式为 .
(2)苯乙烯制取聚苯乙烯的化学方程式为 .
Ⅱ.聚苯乙烯塑料性质稳定,会造成严重的“白色污染”.为此人们开发出一种聚乳酸塑料来替代聚苯乙烯.聚乳酸合成过程如下:

(3)淀粉和纤维素的分子式均可表示为(C6H10O5)n,下列关于淀粉和纤维素的说法正确的是
A.互为同分异构体 B.水解最终产物相同
C.纤维素是纯净物 D.均是高分子化合物
(4)乳酸分子在所含官能团有 (填名称).
(5)根据结构推断聚乳酸可能发生的反应类型是 ,并据此说明用聚乳酸塑料替代聚苯乙烯塑料的好处是 .
(6)乳酸与足量Na反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
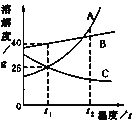
A.t1℃时,B物质的溶解度为40g
B.要将C的不饱和溶液转化为饱和溶液可以采取降温的方法
C.t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C
D.将t2℃时A、B的饱和溶液降温到t1℃时,析出的晶体A比B多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
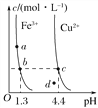
A. Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B. 加适量NH4Cl固体可使溶液由a点变到b点
C. c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D. Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四个反应,其焓变和熵变如下表所示
反应 | A | B | C | D |
ΔH/kJ·mol-1 | 10.5 | 1.80 | -126 | -11.7 |
ΔS/J·mol-l·K -1 | 30.0 | -113.0 | 84.0 | -105.0 |
(1)在任何温度都能自发进行的反应是________;任何温度下都不能自发进行的反应是________。
(2)高温才可以自发进行的反应是________;低温有利于自发进行的反应是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林是日常生活中应用广泛的医药之一,它可由下列方法合成:
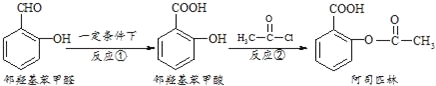
下列说法正确的是( )
A.与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有3 种
B.用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应①
C.邻羟基苯甲醛不能和溴水发生取代反应
D.1mol阿司匹林最多可以和2molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸铵(NH4)2CO3在室温下就能自发的分解产生氨气,对其说法正确的是( )
A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
B.碳酸铵分解是因为外界给予了能量
C.碳酸铵分解是吸热反应,根据能量判据不能自发分解
D.碳酸盐都不稳定,都能自发分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的Fe和Fe2O3混合物投入2mol/L250mL的HNO3溶液中,反应完全后,无固体剩余,生成2.24L(标准状况)NO气体,再向反应后溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
A.400mL B.450mL C.500mL D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com