
设NA表示阿伏加德罗常数的数值,下 列说法正确的是( )
列说法正确的是( )
A.2.4g镁在足量的O2 、CO2、 N2混合气体中燃烧,转移的电子数为0.1NA
B.标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl﹣和ClO﹣两种粒子数之和为NA
C.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
D.标准状况下,20gD2O分子中所含中子数为10NA
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2016-2017学年贵州省高二上10月月考化学卷(解析版) 题型:选择题
将4molA气体和2molB气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)  2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种方法:
2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种方法:
①用物质A表示的反应的平均速率为0.3mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol·L-1
其中正确的是
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上10月月考化学试卷(解析版) 题型:选择题
将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为V1;
②一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为V2;
③一份直接放入足量的盐酸中,充分反应后放出气体在标准状况下的体积为V3。
下列说法正确的是
A.V1=V3>V2 B.V2>V1 =V3 C.V1= V2>V3 D.V1>V3>V2
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第二次月考化学试卷(解析版) 题型:实验题
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ..再经过一系列操作,分离得到产品。
(1)步骤Ⅰ中过滤所得滤渣主要成分为:______________________,
H2SO4溶解Al2O3的离子方程式为:_____________________。
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为: 。
(3)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度均为0.1 mol·L-1
①根据表中数据解释步骤Ⅱ的目的:________________________,
②当Al3+开始沉淀时,Fe3+的浓度约为:_______________________。
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是: 。
②步骤Ⅳ中加入MnSO4的目的是: 。
(5)步骤Ⅴ中“一系列操作”是__________________、_________________。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第二次月考化学试卷(解析版) 题型:选择题
将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,能证明SO2与FeCl3溶液发生氧化还原反应的是( )
操作 | 现象 | |
A | 加入NaOH溶液 | 有红褐色沉淀 |
B | 加入Ba(NO3)2溶液 | 有白色沉淀 |
C | 加入酸性KMnO4溶液 | 紫色褪去 |
D | 加入K3[Fe(CN)6](铁氰化钾)溶液 | 有蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第二次月考化学试卷(解析版) 题型:选择题
将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系是( )

查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上学期第一次模拟化学试卷(解析版) 题型:推断题
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,F元素的原子最外层电子数是电子层数的二倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体、三种是固体。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示) 。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X中所含化学键类型有 。(填数字编号)
①离子键 ②极性键 ③非极性键 ④配位键 ⑤氢键
(4)由A、B两种元素以原子个数比2:1形成的液态化合物Y含有18个电子,其水合物是一种二元弱碱,则Y的电子式为 ;由A、C、F三种元素形成的某化合物能与化合物Y形成一种酸式盐,常温下。1mol/L该酸式盐的pH为1,请写出该酸式盐的化学式 。
(5)化合物Y和A、C形成的18电子分子可相互反应生成两种产物,其中一种产物是空气的主要成分,请写出反应的化学方程式: 。
(6)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上学期第一次模拟化学试卷(解析版) 题型:选择题
将绿豆大小的方形金属钠投入足量且含酚酞的水中,根据相应现象不能得出的结论是( )
选项 | 实验现象 | 结论 |
A | 方形金属钠变成小球 | 方形钠反应速率快 |
B | 钠浮于水面 | 水的密度大于钠 |
C | 酚酞溶液变成红色 | 有NaOH生成 |
D | 钠球游动,有吱吱声 | 有气体产生 |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第一次月考化学试卷(解析版) 题型:选择题
在25 ℃时,将a g NH3完全溶于水,得到V mL pH=8的氨水,假设该氨水的密度为ρ g·cm-3,溶质的质量分数为ω,其中含NH 的物质的量为b mol,下列叙述中一定正确的是
的物质的量为b mol,下列叙述中一定正确的是
A.溶质的质量分数为ω= ×100%
×100%
B.溶质的物质的量浓度c=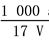 mol·L-1
mol·L-1
C.溶液中c(OH-)=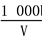 mol· L-1
mol· L-1
D.上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5ω
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com