
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
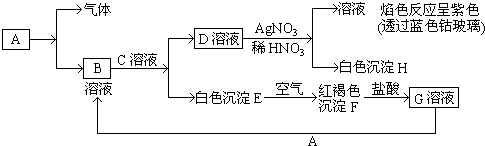
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在25℃,101kPa条件下,11.2L氯气所含的原子数为NA |
| B、2L 0.1mol/L NaCl溶液中含有NaCl分子数为0.2NA |
| C、78g Na2O2与足量CO2完全反应,转移的电子数为2NA |
| D、常温常压下,质量为32g O3含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、状态A时I2的转化率比状态B的小 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C、若反应进行到状态D时,一定有v正>v逆 |
| D、状态A与状态B相比,状态A的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油的分馏是物理变化 |
| B、石油裂化的主要目的是提高汽油的产量和质量 |
| C、石油催化重整的主要目的是得到苯、甲苯等 |
| D、直馏汽油和裂化汽油均可萃取溴水中的溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com