



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
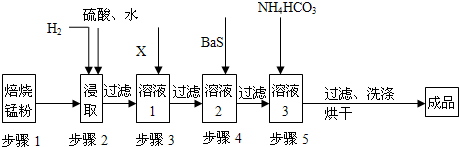
(12��) п�̷ϵ�ؾ���������������������п��̼���̣�����������ҵ��̼���̹������£�

�Իش���������
��1������Ԫ�����ڱ��е� ���ڣ��� �塣
(2)����1�Ͳ���2�ǽ�MnO2��ת��ΪMnO���������ᣬ���в���2�е�����������һ�����̲����ĸ���Ʒ����д�����������ķ�Ӧ����ʽ ��
(3) ����3�Ͳ���4���dz�����
��X��һ�֡���ɫ��������,��X��____________(�ѧʽ)��
�ڲ���3�dz�ȥ����Fe2+���������ֺͱ�Ҫ�ķ���ʽ������ȥFe2+�ķ��� (��֪�������ӳ�����pH��ΧΪFe3+��2.7��3.7��Mn2+��8.6��10.1��Fe2+��7.6��9.6 ��)
___________________________________________________________________________��
�۲���4����Ҫ��Ӧ����ʽΪ��MeSO4+BaS=MeS��+BaSO4��(Me��ҪΪPb��Cd��Hg��)�������ȥ���ʵ�ԭ����______________________________________________��
(4) ��֪���в���5�IJ���ʱ����Һ3(��Ҫ�ɷ�ΪMnSO4)�����������ɫ��ζ�����ݣ�����5��Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com