
 ====2Al(OH)3↓+
====2Al(OH)3↓+ 。
。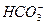 +
+ +H2O====Al(OH)3↓+
+H2O====Al(OH)3↓+
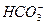 的酸性比Al(OH)3的酸性强,因此可发生反应
的酸性比Al(OH)3的酸性强,因此可发生反应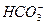 +
+ +H2O====Al(OH)3↓+
+H2O====Al(OH)3↓+ 。
。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源:不详 题型:单选题
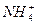 )分别为a、b、c(单位为mol·L-1),则下列判断正确的是( )
)分别为a、b、c(单位为mol·L-1),则下列判断正确的是( )| A.a="b=c" | B.c>a>b | C.b>a>c | D.a>c>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)>c(OH-) |
| B.c(CH3COOH)+c(CH3COO-)=0.2mol·L-1 |
| C.c(CH3COOH)>c(CH3CO1O-) |
| D.c(CH3COO-)+c(OH-)=0.1mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeCl2、FeCl3 |
| B.Na2CO3、NaHCO3 |
| C.NaAlO2、AlCl3 |
| D.Mg(HCO3)2、MgCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.0.1mol·L-1的Na2CO3溶液中离子浓度关系:c(Na+)=2 c(CO )+ c(HCO )+ c(HCO )+ c(H2CO3) )+ c(H2CO3) |
| B.0.1mol·L-1的NH4Cl和0.1mol·L-1的NH3·H2O等体积混合后溶液中的离子浓度关系: c(Cl-)> c(NH  )> c(OH-)> c(H+) )> c(OH-)> c(H+) |
| C.常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系: c(Na+)< c(CH3COO-) |
| D.等物质的量浓度、等体积的NH4NO3和KNO3溶液中,前者的阳离子浓度小于后者的阳离子浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶质为Na2CO3 |
B. |
C. |
D. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com